ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Физико-химические основы процесса
При алкилировании используются различные алкилируюшие агенты и различные катализаторы кислого типа - протонные кислоты: H2SО4, H3PО4, HF, BF3, AlCl3, FeCl3. H2SO4 и HF используются при алкилировании в жидкой фазе при температуре 10-40 °С и давлении 0,1-1,0 МПа. Недостатки - наличие сточных вод и коррозия аппаратуры. А1С13 и FeCl3 - в жидкой фазе при температурах -100 °С и давлении 0,1-1,0 МПа. Недостатки те же. Н3РO4 на носителе используется в газовой фазе при температурах 200-400 °С и давлении 2-6 МПа. Твердые контакты - алюмосиликаты и цеолиты - также работают при высоких температурах при давлении 2-6 МПа.
Для алкилирования бензола и толуола в качестве катализаторов чаще всего используются протонные и апротонные кислоты. Процесс идет в жидкой фазе. Механизм представляет собой реакцию электрофильного замещения в ароматическом ядре. Протекает через стадии диссоциации кислоты, присоединение протона по С=С-связи алкена с образованием карбокатиона. Карбокатион образует с бензольным кольцом сначала π-, а затем σ-комплекс. Реакция завершается отщеплением протона и образованием алкилпроизводного. Если в качестве катализатора используется А1С13, то реакция также идет в присутствии в качестве промотора HCl: В системе образуется нерастворимый в УВ комплекс Густавсона по реакции
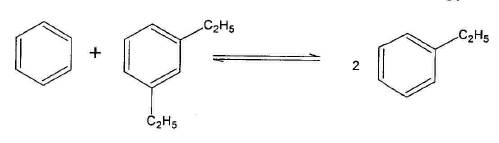
представляющий собой соединение А1Сl3 и НС1 с несколькими молекулами бензола или производных бензола. HCl вводится в систему непосредственно, либо образуется в среде- ароматических углеводородов при гидролизе А1Сl3 в присутствии небольших количеств воды. При катализе реакции комплексом Густавсона может протекать изомеризация гомологов бензола с внутримолекулярной миграцией алкильных групп и образованием равновесной смеси термодинамически более стабильных изомеров. При катализе протонными кислотами алкилирование происходит последовательно с образованием смеси продуктов разной степени алкилирования вплоть до образования гексаалкилбензолов. При низкой температуре до 40-50 °С реакция является необратимой. При катализе А1С13 или алюмосиликатами и цеолитами при высокой температуре протекает реакция переалкилирования, то есть реакция становится обратимой с межмолекулярной миграцией алкильных групп:
В присутствии А1С13 и этих катализаторов (цеолитов и алюмосиликатов) возможен возврат в реактор полиалкилбензолов, где они в результате переалкилирования превращаются в моноалкилбензолы. Реакция переалкилирования является медленной реакцией, протекающей с приемлемой скоростью при температурах - 100 °С. Кроме перечисленных реакций в системе протекает ряд побочных реакций: 1. Деструкция карбокатиона, приводящая к образованию алкиларенов с алкилом меньшей длины. 2. Изомеризация карбокатиона, приводящая к образованию разветвленных заместителей в бензольном кольце.
3. Полимеризация алкенов по катионному механизму, приводящая к образованию смолообразных олигомеров за счет последовательного взаимодействия карбокатиона с алкенами. Их количество увеличивается с ростом концентрации алкенов в жидкой фазе. 4. Смолообразование может происходить также при конденсации ароматических соединений с образованием сконденсированных ароматических ядер. При алкилировании нафталина смол получается больше. Смолообразование увеличивается при росте температуры и удлинении алкильных групп.
Реакции алкилирования и переалкилирования замедляются при разложении каталитического комплекса (в присутствии воды), что ведет к накоплению полиалкилбензолов в реакторе. В свою очередь, накопление полиалкилбензолов и смол также приводит к дезактивации катализатора. Селективность и состав продуктов алкилирования зависит от следующих факторов: 1. Катализатор (его природа и концентрация), 2. Мольное соотношение реагентов (чем больше избыток бензола, тем выше селективность по моноалкилбензолу), 3. Конверсия алкенов, 4. Условия проведения синтеза (температура, давление), 5. Тип реактора, 6. Организация массообмена и теплосъема. В виду того, что процесс алкилирования - гетерофазный, т.е. система состоит из газообразной фазы алкена, и двух несмешивающихся между собой жидких фаз (арен и каталитический комплекс). В связи с этим необходимо осуществление интенсивного перемешивания, чаще всего перемешивание производят барботированием газообразных алкенов через реакционную массу, что ускоряет процесс алкилирования.
|