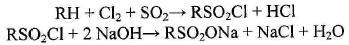ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Технологическая схема синтеза винилацетата из этилена
Смесь свежих и рециркулирующих этилена и уксусной кислоты подогревают в паровом нагревателе 1, смешивают со свежим кислородом и подают в трубчатый контактный аппарат 2 со стационарным слоем катализатора, находящегося в трубах. Выделяющееся тепло отводят за счет испарения (в межтрубном пространстве) водного конденсата; при этом вырабатывают пар, отделяемый в сборнике 3. Реакционную смесь охлаждают в холодильнике 4 и промывают газ последовательно в скрубберах 5 и 6 рециркулирующей уксусной кислотой и водой для улавливания соответственно винилацетата и уксусной кислоты. Большую часть промытого газа возвращают циркуляционным компрессором 7 на синтез, но часть его проходит блок 8 карбонатной очистки от СО2. Очищенный газ большей частью рециркулируют, но некоторое его количество выводят из системы, чтобы избежать чрезмерного накопления инертных примесей, содержавшихся в этилене и кислороде. Смесь жидких продуктов из куба скрубберов 5 и 6 направляют на разделение в систему ректификационных колонн 9, где отделяются винилацетат, вода, уксусная кислота и тяжелые примеси, направляемые на сжигание.
Получение этиленгликолядиацетата
Процесс идет на твердом катализаторе PdCl2+CuCl2 на носителе. Реактор трубчатый. В результате образуется смесь, состоящая из диацетата этиленгликоля 60 %, моноацетата этиленгликоля 30 % и этиленгликоля 10 %. Далее полученную смесь подвергают гидролизу c образованием этиленгликоля, а уксусную кислоту направляют в рецикл. Выход ЭГ 90 %. Себестоимость выше чем при гидратации ОЭ. Сложные эфиры ДАЭГ и МАЭГ используют как пластификаторы. ГАЛОГЕНИРОВАНИЕ
ПРОЦЕССЫ СУЛЬФАТИРОВАНИЯ И СУЛЬФИРОВАНИЯ Сульфатирование - это процессы образования сложных эфиров серной кислоты (алкилсульфатов)
Сульфирование -это процессы образование сульфокислот: R-SО2OH. Соли этих кислот сульфаты и сульфонаты при достаточной длине алкильного заместителяпроявляют поверхностно-активную природу. Большее применение имеют натриевые соли сульфатов и сульфонатов - это основа современных моющих средств
Процессы сульфатирования
Сульфатированию подвергаются жирные спирты (в основном первичные) и a-алкены, т.к. гидрофобная часть должна быть неразветвленной. Кроме того, сульфатированию подвергаются оксиэтилированные жирные спирты – синтанолы
Сульфатирующими агентами являются H2SО4 конц., олеум (SО3 в H2SО4 конц), хлорсульфоновая ClSO2OH и сульфаминовая H2NSO2OH кислоты.
Сульфатирование спиртов
Накопление в системе воды приводит к торможению процесса и ее необходимо отводить. Реакция сильно экзотермична, тепловой эффект зависит от концентрации H2SO4. Выход алкилсульфокислоты - 60-65 %. Реакционная способность спиртов уменьшается в ряду: первичный > вторичный >третичный Синтез ведут в избытке H2SО4 (1,8-2,0) кратном при температуре 0-20 °С. Наряду с основной реакцией в кислой среде идет реакция дегидратации спиртов (внутри- и межмолекулярная). Образующиеся алкены могут полимеризоваться с образованием смолообразных продуктов (катионная полимеризация). Спирты и H2SО4 плохо смешиваются друг с другом, поэтому необходимо тщательное перемешивание. Чаще используют пленочные аппараты, где процесс идет в тонком слое, с целью облегчения теплосъема. При использовании в качестве сульфатирующего агента сульфаминовой кислоты эта реакция становится необратимой
Реакция с сульфаминовой кислотой используется чаше всего для сульфатирования оксиэтилированных фенолов и ненасыщенных спиртов (недостаток – дорогой сульфатирующий агент) С хлорсульфоновой кислотой
При связывании HCl процесс становится практически необратимым. С олеумом
Так как тепловой эффект очень большой, скорость реакции ограничивают за счет разбавления SО3 инертным газом или воздухом. Технологическая схема получения алкилсульфатов из спиртов и SO3
Технологическая схема производства моющего средства на основе алкилсульфата изображена на рис. . В пленочный реактор 1 непрерывно подают спирт, воздух и пары SO3, разбавленные воздухом. Выходящие газы отделяют в сепараторе 2 от жидкости и направляют в абсорбер 3 для санитарной очистки от остатков SO3. Полученную алкилсерную кислоту нейтрализуют концентрированным раствором щелочи в аппарате 4, имеющем мешалку и выносной холодильник 5, через который жидкость прокачивается насосом. Температура при нейтрализации не должна превышать 60°С. После этого в аппарате 6 с мешалкой проводится более точная нейтрализация смеси (до рН 7; контроль специальным рН-метром). Нейтрализованная масса, содержащая алкилсульфат и воду, поступает далее в смеситель 7, где к ней добавляют другие компоненты моющего средства (фосфаты или дифосфаты, сода, отбеливатели, карбоксиметилцеллюлоза). Эту смесь подают насосом в распылительную сушилку 8, вбрызгивая ее через специальные сопла в поток горячего топочного газа. Унесенные газом твердые частицы улавливают в циклоне 9. Порошкообразное моющее средство с низа сушилки и циклона транспортируют шнеком 10 на расфасовку.
Сульфатирование алкенов
При взаимодействии a-алкенов с сульфатирующими агентами, например с серной кислотой образуются вторичные сульфаты
Если в H2SО4 имеется вода, то в системе могут протекать побочные реакции - могут быть полимеры, простые эфиры. Концентрация H2SО4 должна быть 92-94 %. Соотношение алкен : H2SO4 ~ 1 температура 0-40 °С. Технология сходна с получением алкилсульфатов из спиртов. Чаще - в пленочном аппарате, может использоваться каскад аппаратов с мешалками и охлаждением рассолом. Для ПАВ, полученных из спиртов оптимально использовать C12-С16, для алкенов может быть C16-С18.
ПРОЦЕССЫ СУЛЬФИРОВАНИЯ
Подвергаются алкены, алкилароматические соединения
Сульфирующими агентами являются концентрированная серная кислота, олеум, SO3. Сульфирование алкилароматических соединений
Вторую сульфогруппу в бензольное кольцо ввести достаточно сложно. Аналогично идет реакция с SO3 10-40 °С, реакция экзотермична. Побочно протекает реакция образования сульфонов
Могут образовываться ангидриды сульфокислот
Кроме того, могут протекать реакции конденсации ароматических соединений, приводящие к образованию смолообразных окрашенных продуктов, что вызывает потемнение ПАВ (нежелательно). Чаще всего алкилсульфонаты в промышленности получают при взаимодействии алкилбензолов с SO3.
Это производство обычно комбинируют с частичным окислением SO2 в SО3 техническим кислородом в блоке 1. Продукты после охлаждения и конденсации в холодильнике 2 собирают в сборнике 3 в виде 10-15 %-го раствора SО3 в жидком SO2. Этот раствор, а также раствор алкил-ароматического углеводорода в жидком SO2 вводят на тарелку (стакан) реактора 4 он перетекает на стенку корпуса (разбрызгивается мешалкой), и там в стекающей вниз пленке реакция завершается. Жидкость, выходящая из реактора, еще содержит 5-7 % SО2, и для удаления последнего ее подогревают и направляют в вакуумный испаритель 5, после чего она стекает в сборник 7 и поступает на дальнейшие стадии переработки (нейтрализация, смешение, сушка, расфасовка). рис. 92. Газообразный SO2 с верха реактора и испарителя возвращают в блок 1.
Длина алкильной цепи в бензольном кольце С10-С16 (получают алкилированием бензола либо хлорпроизводными, либо a-алкенами). Такие сульфонаты называют сульфонолы (синтетические). Кроме этого в промышленности получают нефтяные сульфонолы. В синтетических используют индивидуальные галогенпроизводные, а в нефтяных хлорированию подвергают соответствующие фракции нефти
Для алкилирования используют всю эту смесь, далее осуществляют сульфирование. Эти сульфонолы худшего качества (разные длины, могут быть разветвления) - используются как эмульгаторы. Алкилсульфонаты можно получать также с помощью процессов сульфохлорирования и сульфоокисления алканов.
СУЛЬФОХЛОРИРОВАНИЕ
Реакция сильно экзотермична и необратима, протекает при 30-70 °С в каскаде барботажных колонн или в секционированной тарельчатой колонне со встроенными ртутными лампами. Используют испаренный хлор. Сырье не должно содержать примесей сернистых соединений и других ингибиторов радикальных процессов.
Побочные продукты - хлорпроизводные (3-5 %). Подавлению хлорирования способствует избыток SO2 (5-10 %). При сульфохлорировании н-алканов С12-18 получаются в основном вторичные сульфохлориды. В реактор вводят свежие и рециркулирующие алканы, через которые барботируют хлор и SO2. Далее в отдувочной колонне удаляют растворенные HCl и SО2. Газовая фаза выводится на абсорбцию с получением соляной кислоты и санитарную очистку. Смесь нейтрализуют, в сепараторе отделяют непревращенные RH, возвращаемые на сульфохлорирование. Водный раствор охлаждают до 5-10 °С, при этом алкилсульфонаты собираются вверху в виде клейстера. Нижний водный слой содержит до 20 % алкилсульфонатов, которые экстрагируют спиртом. Клейстер разбавляют водой до 20 %-ной концентрации и отбеливают хлором (разрушают смолы). Раствор выпаривают под вакуумом с получением готового продукта в виде 50-60 % водного раствора алкилсульфонатов.
СУЛЬФООКИСЛЕНИЕ
RH – парафины C12-18. Реакция сильно экзотермична и необратима. Радикально-цепной механизм, температура 25-30 °С, но квантовый выход меньше, чем в процессе сульфохлорирования.
Кинетическая цепь более короткая, чем при сульфохлорировании (5-10), что требует значительных затрат на облучение (инициирование). В аппаратах устанавливают ртутные лампы для УФ облучения. Побочные реакции - окисление (особенно у изо-алканов и алкиларенов). Получаются в основном вторичные алкилсульфонаты. При сульфохлорировании расходуется много щелочи и хлора, теряемые в виде NaCl, а при сульфоокислении - SО2 (серная кислота). По себестоимости сульфохлорирование и сульфоокисление примерно сопоставимы. Чем ближе находится сульфонатная группа к концу углеродной цепи, тем лучше ПА свойства продукта. Максимальной ПАС обладают сульфонаты с прямой цепью из 14-16 углеродных атомов, чем определяется выбор сырья (керосиновая фракция парафинистой нефти или мягкие парафины, выделенные при помощи цеолитов или карбамида). Алкилсульфонаты по своим поверхностно-активным и моющим свойствам уступают алкилсульфатам и сульфонолам, особенно в жесткой воде. Вследствие клейкости и слабой кристалличности алкилсульфонаты используются в виде водных растворов в качестве эмульгаторов, жидких мыл и добавок к другим моющим веществам. На алкилсульфонаты приходится 3-5 % от общего производства анионных ПАВ.
ПРОЦЕССЫ НИТРОВАНИЯ
Нитросоединения используются в качестве взрывчатых веществ. Они являются исходными веществами для синтеза аминов, для получения лекарственных средств, средств защиты, растений. Практическое значение имеет нитрование ароматических соединений и насыщенных углеводородов.
|