 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Основные этиологические формы панкреатитов
Вэтом разделе мы рассмотрим наиболее часто встречающиеся этиологические причины развития ХП: алкоголизм, патологию желчевыводящих путей и двенадцатиперстной кишки, наследственные факторы, лекарственные поражения ПЖ, а также идиопатический ХП. 2.2.1. Алкогольный панкреатит и курение Один из первых случаев алкогольного панкреатита был описан в 1788 г. Cawley, который наблюдал молодого «беспечно живущего» мужчину, погибшего от истощения и сахарного диабета. На вскрытии в поджелудочной железе были выявлены многочисленные камни (цит. по [43]). В настоящее время алкоголизм среди множества причин хронического панкреатита, по данным и зарубежных [190, 258, 277, 519], и отечественных [1, 37, 59] исследователей, составляет 40—80 % случаев. На сегодняшний день установлено, что злоупотребление алкоголем служит основной причиной развития ХП в индустриально развитых странах [258, 519]. Наблюдается линейная зависимость между потреблением алкоголя и логарифмическим риском развития ХП [182, 190]. Отмечена прямая корреляция между заболеваемостью панкреатитом и потреблением алкоголя мужчинами в возрасте 20—39 лет [50]. Однозначного мнения о том, какая доза этанола способствует развитию заболевания, в настоящее время нет. Разные авторы указывают, что ХП развивается при употреблении этанола в количестве от 20 до 100 г в сутки в течение от 2 до 20 лет [190, 258, 277, 459]. В развитых странах длительный прием (6—18 лет) этанола в дозе более 150 мг/сут отмечают 60—70 % больных ХП [43]. В то же время установлено, что употребление алкоголя на протяжении 8—12 лет даже в дозе 80—120 мл в сутки приводит к развитию изменений в ПЖ, чаще всего кальцинозу и накоплению жира в аци-нарных клетках [20]. Сообщается, что риск развития ХП для непьющих более низок, чем риск для людей, употребляющих даже малые количества этанола (до 20 г в сутки). На основании полученных данных авторами был сделан вывод, что не существует никакого статистического порога для токсичности алкоголя, а ведущее значение имеют факт ежедневного употребления алкоголя и общая продолжительность его употребления [191]. Считается, что существуют т. н. «безопасные» дозы алкоголя для ПЖ. А. И. Хазанов приводит данные, что 210 мл чистого этанола в неделю является такой безопасной в отношении развития ХП дозой. Имеются данные, что опасными и очень опасными дозами являются соответственно 80—160 и более 160 мл чистого этанола в сутки [72]. Некоторые панкреато-логи считают, что токсическая доза для ПЖ в 2 раза больше, чем для печени; панкреотоксическая доза этанола для женщин в 2 раза меньше, чем для мужчин [42]. Глава 2. Этиология и патогенез хронического панкреатита • 29
Так, исследования Т. Kondo и соавт. [301] показали, что помимо алкогольного воздействия для развития панкреатита необходимо сочетанное воздействие различных факторов, включающих анатомические особенности ПЖ, особенности кровоснабжения и иннервации, строения протоко-вой системы железы, а также особенности питания. Эта концепция в последние годы была серьезно оспорена [434]. По результатам исследований, проведенных в Японии, риск возникновения ХП был выше у лиц, употребляющих низкоалкогольные напитки [356]. Интересны экспериментальные данные Н. Sarles и соавт. (1971), показавших более высокую частоту возникновения ХП у крыс при длительном введении в рацион питания высокого содержания белка и алкоголя [428]. В отдельных исследованиях Н. Tsukamoto и соавт. (1988) было показано, что у крыс на фоне уменьшения доли жиров в пище хроническая алкогольная интоксикация приводила к значительно менее выраженным изменениям в ПЖ. Достоверно более выраженные морфологические изменения были отмечены в группе животных, получавших, помимо стандартных доз алкоголя, корм с высоким содержанием жиров [482]. Большая вариабельность данных о дозах и сроках употребления алкоголя, приводящих к развитию ХП, позволила предположить, что существует генетическая предрасположенность к ХП [247]. Нельзя игнорировать и тот факт, что, в отличие от лиц европеоидной расы, представители негроидной расы госпитализируются по поводу обострения хронического алкогольного панкреатита в 2—3 раза чаще, чем по поводу алкогольного цирроза печени [328]. Интерес представляет географическое распространение алкогольного панкреатита. Чаще всего этот вид панкреатита встречается во Франции, Италии, Швейцарии и значительно реже в Германии, Дании, Швеции, Чехии, Словакии и Аргентине. Промежуточное положение занимает Великобритания. В последние ходы отмечается рост заболеваемости алкогольным панкреатитом в Японии [59, 356], несмотря на относительно низкие показатели потребления этанола в обществе. Алкогольный панкреатит встречается чаще у мужчин в возрасте 35—45 лет. Частота выявления ХП при аутопсии интенсивно пьющих людей достигает 45—50 %. Более чем у 50 % лиц, страдающих алкоголизмом, наблюдаются нарушения экзокринной функции ПЖ [153]. Существуют данные, что при сочетании алкогольного поражения печени и pancreas внешнесек-реторная недостаточность последней выражена в большей степени, чем при изолированном алкогольном хроническом панкреатите [15]. Механизм возникновения хронического панкреатита на фоне приема алкоголя не до конца изучен. Считается, что в патогенезе алкогольного панкреатита участвуют несколько механизмов [13]: 1. Этанол вызывает спазм сфинктера Одди, в результате чего возникает внутрипротоковая гипертензия и стенки протоков становятся проницаемыми для ферментов [74]. Последние активируются под действием лизосо-мальных гидролаз, «запуская» аутолиз ткани ПЖ. Так, в исследованиях R. Laugier и соавт. (1998) у больных алкогольным ХП орошение области большого дуоденального сосочка раствором этанола приводило к значительно-
2. Было установлено, что под влиянием алкоголя изменяется качествен 3. Этанол нарушает синтез фосфолипидов клеточных мембран, вызывая 4. Этанол угнетает биоэнергетические процессы в клетках, уменьшая их 5. Первичным метаболитом алкоголя является уксусный альдегид, ока 6. Этанол способствует фиброзу мелких сосудов с нарушением микро
При воспроизведении модели хронического алкогольного панкреатита на крысах было установлено, что алкоголь инициирует фиброзный процесс в ПЖ, сопровождающийся уменьшением доли ацинарной ткани, снижением массы органа, ростом уровня глюкозы крови [129, 484]. Необходимо отметить, что имеет значение не путь введения алкоголя в организм, а его концентрация в крови. Следует также учитывать, что желчь у больных ХП, страдающих алкоголизмом, обладает выраженным панкреотоксическим эффектом из-за повышенного содержания в ней свободных желчных кислот [67]. Показано возрастание риска развития хронического алкогольного панкреатита при наличии дополнительного фактора — курения. Более того, в этом случае панкреатит развивается в более раннем возрасте [49]. В последние годы стало известно, что ХП у курящих наблюдается в 2 раза чаще по сравнению с некурящими субъектами [459], и риск развития заболевания растет в зависимости от количества выкуриваемых сигарет [519]. Курение сигарет приводит к истощению запасов витаминов С и А, а также снижает сывороточный уровень других антиоксидантов, что обусловливает повреждение ткани железы свободными радикалами [361, 415, 485]. Так, в рамках National Health and Nutrition Examination Survey III Глава 2. Этиология и патогенез хронического панкреатита • 31
Нельзя не учитывать результаты исследования Research Committee on Intractable Pancreatic Diseases (Япония), когда изучалась взаимосвязь потребления алкоголя и особенностей нутритивного статуса у больных хроническим алкогольным панкреатитом. В рамках этой программы с июля 1997 г. по декабрь 1998 г. был обследован 91 больной ХП (все мужчины) с недавно диагностированным ХП и 175 лиц контрольной группы. Результаты исследования показали, что потребление витамина Е имело отрицательную корреляционную связь с риском развития ХП (р = 0,03) [322]. По данным С. S. Liu и соавт., курильщики старшее 45 лет имеют существенно более низкие плазменные уровни аскорбатов (0,32 ± 0,17 мг/дл), чем некурящие (0,53 ± 0,14 мг/дл) (р = 0,036) [324]. Результаты экспериментальных исследований К. Panda и соавт. показывают, что прием 100 мг аскорбиновой кислоты практически полностью предотвращает индуцированное сигаретным дымом окисление белка и таким образом защищает микросомы от последующей протеолитической деградации [382]. Следует отметить, что комбинация антиоксидантов (витамины Е и С, липоевая кислота) более эффективна в плане профилактики у курильщиков, чем монотерапия витамином С [181]. При кросс-секционном исследовании связи между курением сигарет и состоянием в крови микронутриентов у пожилых людей, проживающих в Великобритании (National Diet and Nutrition Survey) было обследовано 1191 человек (619 мужчин и 572 женщины) старше 65 лет. Было показано, что курение сигарет обратно коррелировало с большинством индексов ан-тиоксидантного статуса, включая уровень в плазме витамина С и каротинов [324]. Интересны результаты исследований A. J. Alberg и соавт., которые определили, что даже у пассивных курильщиков имеются более низкие сывороточные концентрации каротиноидов, альфа-каротина, ретинола, альфа-и гамма-токоферолов, криптоксантина, чем у лиц, проживающих в доме без курильщиков [85]. Аналогичные данные, свидетельствующие о низких плазменных концентрациях аскорбиновой кислоты у пассивных курильщиков, получены в исследовании, проведенном в Японии, и свидетельствуют о наличии оксидативного стресса при пассивном курении [97]. R. А. Jacob предлагает профилактический прием аскорбиновой кислоты в качестве антиоксиданта для минимизации вредных воздействия сигаретного дыма у пассивных курильщиков [276]. Экспериментальные данные, полученные в Центре генной инженерии и биотехнологий доктора В. С. Guha и на кафедре биохимии научно-исследовательского института Калькуттского университета (Индия), указывают, что сигаретный дым вызывает окислительное повреждение легких, сердца и печеночных микросоматических белков. Данный эффект почти полностью предотвращался аскорбиновой кислотой. Полная защита против данных эффектов происходила при употреблении 15 мг витамина С [381]. Известно, что антиоксидантная терапия уменьшает отрицательные эффекты на кровоток при курении, устраняя дисбаланс между прооксидант-ными и антиоксидантными системами. В исследованиях J. Zhang и соавт. был изучен эффект курения на микроциркуляцию у 24 практически здоровых пациентов. Было выявлено ухудшение микроциркуляции у 23 из 24 че- 32 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
Курение сигарет снижает панкреатическую секрецию бикарбонатов [132], что приводит к повышению вязкости панкреатического сока [151]. В этих условиях также возможна преципитация белка с закупоркой просвета протоков ПЖ белковыми пробками с развитием локальной панкреатической гипертензии по описанному выше механизму. Существуют данные о снижении активности ингибитора трипсина у курильщиков [151], что повышает риск внутрипротоковой активации ферментов. Имеются сообщения и о снижении уровня оц-антитрипсина в сыворотке крови курильщиков. Известен факт развития первичного ХП на фоне врожденного дефицита а,-антитрипсина [344], однако нельзя исключить возможность развития ХП и при приобретенном дефиците оц-анти-трипсина, что требует проведения дальнейших исследований. 2.2.2. Билиарнозависимый панкреатит и заболевания гастродуоденальной зоны 2.2.2.1. Заболевания желчевыводящих путей и гастродуоденальной зоны как причинный фактор развития хронического панкреатита Среди причинных факторов ХП патология желчевыводящих путей имеет место в 35—56 % случаев. В Европе желчнокаменная болезнь является причиной развития от 30 до 50 % случаев ОП [163, 171, 333, 472]. Вовлечение ПЖ в патологический процесс при хроническом холецистите и желчнокаменной болезни зависит от давности заболевания и локализации конкрементов [20], встречается чаще у женщин [65]. Кроме того, причиной развития билиарнозависимого панкреатита являются врожденные аномалии желчевыводящих путей, кисты холедоха, патология фатерова сосочка двенадцатиперстной кишки [24, 45]. В основе этого этиологического варианта ХП лежит гипотеза «общего протока» (common channel), предложенная еще Е. Opie в 1901 г. [378]. После того как Е. Opie обнаружил камень в фатеровом сосочке у пациента, умершего от острого панкреатита, он предположил, что анатомическая близость мест впадения желчного и панкреатического протоков в двенадцатиперстную кишку в силу разнообразных причин может приводить к рефлюксу желчи в панкреатический проток, что приводит к повреждению ПЖ детергентами, содержащимися в желчи. Вследствие обструкции протока или ампулы дуоденального сосочка развивается гипертензия в ГПП с последующим разрывом мелких панкреатических протоков. Это приводит к выделению секрета в паренхиму железы, активации пищеварительных ферментов, что в свою очередь ведет к развитию деструктивно-дегенеративных изменений в ПЖ. Следует отметить, что обструкция большого дуоденального сосочка может быть как стойкой, так и преходящей. На первых этапах заболевания
это обусловлено микролитиазом, приводящим к папиллоспазму, причем дисфункциональные расстройства сфинктера Одди значительно чаще возникают у лиц, перенесших холецистэктомию [220]. Конечным итогом всех перечисленных состояний является развитие стеноза терминального отдела общего желчного протока, большого дуоденального сосочка, устья ГПП, что приводит к стойкой гипертензии в общем желчном и главном панкреатическом протоках [66, 161, 162, 220, 265]. Частые рецидивы билиарного панкреатита обычно возникают при миграции мелких и очень мелких камней (микролитов) (табл. 2.1) [73, 346]. Среди микролитов наиболее опасными являются камни размером до 4 мм [155]; наличие в желчном пузыре конкрементов менее 5 мм в диаметре увеличивает риск развития панкреатита в 4 раза [180]. В контексте обсуждаемой проблемы большое значение в развитии ХП придают билиарному сладжу, частота выявления которого у больных идиопатическим ХП, по данным разных авторов, достигает 33—75 % [100, 144, 300, 440]. Примечательно, что у больных панкреатитами алкогольной этиологии билиарный сладж выявляется значительно реже — в 8—15 % случаев [144]. В целом холедохолитиаз является одной из главных причин развития хронического билиарнозависимого панкреатита; по данным разных авторов, частота развития ХП на фоне холедохолитиаза колеблется в пределах 25—65,3 % [1, 26, 51]. Значительные колебания частоты ассоциации холедохолитиаза и билиарного ХП зачастую связаны с тем, что преходящие эпизоды обострения ХП расцениваются как проявления холедохолитиаза, а не как клиническая картина билиарнозависимого ХП [308]. Существует мнение, что не всякий холедохолитиаз приводит к развитию билиарнозависимого ХП, чаще это ампулярный литиаз и конкременты большого дуоденального сосочка [101]. Частота ампулярного литиаза составляет 20— 25 %. Подавляющее количество камней в фатеровом сосочке имеют желчное происхождение, однако есть сообщения и о панкреатогенном литиазе с развитием панкреатита и желтухи [1]. Если давать оценку в целом, то женщины страдают холелитиазом в 2— 6 раз чаще мужчин [4]. В последние годы в странах Европы и Северной Америки отмечена тенденция к уменьшению числа билиарных панкреатитов, что, по-видимому, связано с проведением более ранних операций при возникновении обострения хронического калькулезного холецистита и достаточно широким применением литолитической терапии [111, 489]. Однако любая операция, выполненная по поводу ЖКБ или ее последствий, связана с развитием в дальнейшем сложных патофизиологических процессов, приводящих к нарушению переваривания и всасывания пищи [63]. В последние годы появились указания, что для развития ХП необходимы патологические изменения самой желчи, которую М. И. Кузин и соавт. 34 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
Одним из механизмов развития хронического билиарного панкреатита является лимфогенное поражение ПЖ, преимущественно головки; источником поражения является цепь увеличенных лимфатических узлов, идущих от воспаленного желчного пузыря к головке ПЖ [67]. Справедливости ради следует сказать, что не всеми исследователями принимается билиарная теория возникновения ХП [105]. Имеются данные, что без нарушения оттока желчь не вызывает развитие панкреатита [1]. Рядом авторов теория «общего канала» вообще оспаривается как таковая, поскольку в норме давление в системе панкреатических протоков выше, чем в желчевыводящих путях, что у лиц без патологии в данной области препятствует возникновению рефлюкса желчи в протоки ПЖ. Сам реф-люкс, возникающий в ходе ЭРХПГ, далеко не всегда вызывает обострение панкреатита. Одним из главных защитных механизмов является слизистая оболочка ГПП, резистентная при нормальном давлении к желчи и даже к ее смеси с панкреатическим секретом. В то же время было показано, что длительная инкубация желчи в смеси с панкреатическим секретом или культурой бактерий существенно изменяет состав желчи. Воздействие на желчь панкреатических ферментов, в частности фосфолипазы и бактериальных токсинов, освобождает ранее связанные лизолецитин, желчные кислоты, при этом желчь приобретает отчетливо повреждающее действие на защитный барьер протоков ПЖ. Было замечено, что указанным изменениям значительно легче подвергается желчь больных, страдающих желчнокаменной болезнью [37]. Некоторые западные исследователи не выделяют билиарный панкреатит в отдельную нозологическую форму и расценивают случаи панкреатита у больных холелитиазом без других этиологических факторов как идиопати-ческий панкреатит. В то же время последние данные подтверждают значение билиарной патологии в возникновении ХП вследствие функциональных и органических изменений сфинктера Одди и ампулы фатерова сосочка [45]. При ХП, связанном с патологией большого дуоденального сосочка, нарушения оттока панкреатического секрета и восходящее инфицирование ПЖ с дальнейшим вовлечением в процесс протоковой системы, а затем и паренхимы последней, оказываются обусловлены поражением самого сосочка и при возможном отсутствии изменений со стороны желчи [52]. Патология большого дуоденального сосочка включает функциональные нарушения и органическую патологию сфинктера (папиллит, аденома фатерова сосочка, несостоятельность вследствие папиллосфинктеротомии, парафа-теральный дивертикулез с дивертикулитом и др.). Ухудшают имеющиеся нарушения заболевания двенадцатиперстной кишки с явлениями дуодено-стаза и замедлением эвакуации (синдром функциональной неязвенной диспепсии, язвенная болезнь, дуодениты, стенозирующие опухоли двенадцатиперстной и проксимального отдела тощей кишки, рубцово-язвенные сужения двенадцатиперстной кишки, сдавление дуоденального перехода Глава 2. Этиология и патогенез хронического панкреатита • 35
Механизм развития ХП у больных с данной патологией общий — проникновение в протоки поджелудочной железы желчи либо кишечного содержимого с интрапанкреатической активацией ферментов. Первое сообщение о стенозе большого дуоденального сосочка появилось в 1884 г., когда С. Landenbuch для извлечения вклиненного в фатеров сосочек камня был вынужден рассечь сосочек в связи с его рубцовым стенозом. «Склероретрактильный оддит» описали в 1926 году D. Del Valle и R. Donovan как причину механической желтухи при отсутствии камней в желчном пузыре. По имени этих авторов первичный стенозирующий па-пиллит называют болезнью Дель-Вале-Донована [9]. Этиология первичного стеноза большого дуоденального сосочка до сих пор не ясна, а хронический билиарнозависимый панкреатит развивается при данной патологии в 34—48 % случаев, что приблизительно соответствует частоте встречаемости единой ампулы общего желчного и панкреатического протоков. Вторичный стеноз большого дуоденального сосочка появляется чаще всего после травматизации последнего при прохождении мелких конкрементов, а также вследствие патологических изменений двенадцатиперстной кишки или слизистой оболочки желчевыводящего протока [1]. Достаточно частой причиной, приводящей к развитию ХП, является дуоденопанкреатический рефлюкс, возникающий на фоне недостаточности сфинктера Одди, особенно при наличии дуоденостаза [1, 51]. Причиной атонии большого дуоденального сосочка является папиллит, чаще возникающий после прохождения конкрементов [37], или общая дисмоторика двенадцатиперстной кишки [34], которая может носить функциональный характер [23], либо возникать вторично на фоне органической патологии двенадцатиперстной кишки и соседних органов, как было сказано выше. Хроническая дуоденальная непроходимость функционального характера приводит к дискоординации сфинктерного аппарата большого дуоденального сосочка с его преходящей недостаточностью и рефлюксом дуоденального содержимого как в общий желчный проток, так и в ГПП. Замыкает порочный круг патогенеза ХП дуоденальная гипертензия, потенцирующая стаз в желчном и панкреатическом протоках. Следует отметить, что в значительном числе случаев имеет место комбинация этиологических механизмов в развитии билиарнозависимого ХП; например, у больных желчнокаменной болезнью и холелитиазом с достаточно большой частотой выявляются опухоли БДС и периампулярной зоны [294], либо наличие язвенной болезни у больных желчнокаменной болезнью [45]. Существуют указания на развитие ХП вследствие хронической пенетри-рующей язвы желудка или двенадцатиперстной кишки [3, 67]. В целом, считается, что язвенная болезнь двенадцатиперстной кишки в 10,5—16,5 % случаев является непосредственной причиной развития ХП [33]. Патогенетическим фактором является отек фатерова сосочка (папиллит) с вторичным затруднением оттока панкреатического секрета. Существует мнение, что преходящие папиллиты, встречающиеся при дуоденитах и рецидивах язвенной болезни двенадцатиперстной кишки, могут приводить в дальнейшем к дисфункциональным нарушениям сфинктера Одди, что способствует ухудшению оттока панкреатического секрета даже в период ремиссии язвенной болезни [13]. Вторым патогенетическим механизмом развития ХП у больных язвен- 36 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
В развитии панкреатита при анацидных состояниях играют роль замедление пассажа кишечного содержимого, бактериальная контаминация тонкой кишки с избыточным бактериальным ростом и инвазией микроорганизмов в составе дуоденального рефлюктата в ГПП [45]. В последнее время появляется все больше публикаций, предполагающих участие Helicobacter pylori в развитии и прогрессировании ХП, о чем мы более подробно поговорим в следующем разделе монографии. 2.2.2.2. Панкреатиты и инфекция Helicobacter pylori Начиная с первого описания инфекции Helicobacter pylori (HP) в слизистой оболочке желудка Уорреном и Маршаллом [500], значение данного открытия прогрессивно повышалось; в настоящее время HP признан ведущим этиопатогенетическим фактором развития хронического гастрита, язвенной болезни и рака желудка. В последние годы появляется все больше данных о связи HP с различными внежелудочными заболеваниями. Перси-стирующая HP-инфекция вызывает изменения физиологии верхних отделов ЖКТ. Влияние HP на физиологию экзокринной паренхимы ПЖ, а также на развитие и профессирование заболеваний ПЖ до сих пор исследованы недостаточно. Такая взаимосвязь теоретически возможна, поскольку имеются тесные анатомо-физиологические взаимосвязи между желудком, двенадцатиперстной кишкой и ПЖ, а влияние HP на физиологию желудка и двенадцатиперстной кишки общеизвестно [331]. Влияние HP на физиологию ПЖ.Поиск возможных механизмов, посредством которых HP-инфекция может влиять на физиологию ПЖ, был целью нескольких исследований. Афессивное воздействие HP на слизистую оболочку желудка обусловлено выделением целого ряда факторов (аммиак, липополисахариды) и активацией лейкоцитов с гиперэкспрессией провоспалительных цитокинов. Каждый из этих факторов может изменять физиологию ПЖ и влиять на профессирование различных заболеваний pancreas. J. Jaworek и соавт. [279] изучали влияние интрадуоденального NH4OH на плазменные уровни гастрина и секрецию ПЖ у собак с панкреатической фистулой. Кроме того, был оценен эффект NH4OH на секреторную деятельность in vitro изолированных ацинусов, полученных из ПЖ крысы. Авторы определили, что интрадуоденальное введение NH4OH существенно и дозозависимо увеличивает синтез белка в экзокринной паренхиме и вызывает повышение плазменных концентраций гастрина. Точно так же в изолированных панкреатических ацинусах при увеличении концентрации NH4OH отмечена модуляция выделения амилазы. Авторы заключили, что, в то время как NH4OH стимулирует базальную панкреатическую секрецию, вероятно посредством увеличенного выделения гастрина, ингибирование NH4ОН-стимулированной секреции, обусловлено, по крайней мере, частично, его прямым действием на панкреатические ацинусы, возможно, из-за их ощелачивания. Y. Hori et al. [266] исследовали эффект вакуолизирующего токсина HP на секрецию ферментов в изолированных ацинусах крысы. Авторы выяви- Глава 2. Этиология и патогенез хронического панкреатита • 37
В двух исследованиях [266, 279] изучались эффекты изолированных компонентов бактерии, аммиака и вакуолизирующего токсина HP на ПЖ. Было выявлено стимулирующее влияние HP на панкреатическую секрецию. Известно, что HP ингибирует синтез и выброс желудочными D-клет-ками соматостатина [343, 374, 404], что сопровождается сокращением ан-тральной плотности D-клеток с возвратом их числа к норме после эради-кации HP [404]. Следствием HP-индуцированного ингибирования синтеза и выделения соматостатина является увеличение плотности G-клеток и синтеза гастрина в антральном отделе желудка. Результат всех указанных гормональных изменений — увеличение желудочной кислотной секреции без изменения чувствительности париетальных клеток к гастрину [200, 285, 359, 390]. Известно, что экзокринная панкреатическая секреция ингибируется со-матостатином [185, 251]. Паракринный эффект соматостатина в слизистой оболочке желудка, вряд ли, может влиять на панкреатическую секрецию. Однако, ацидификация двенадцатиперстной кишки может стимулировать панкреатическую секрецию посредством выделения секретина [249]. Кроме того, гастрин проявляет слабый ХК-подобный эффект на панкреатическую секрецию [447]. В недавнем исследовании [184], выполненном на группе из 19 здоровых добровольцев (11 HP-позитивных), было определено, что и HP-позитивные, и HP-негативные субъекты имели нормальную циклическую межпищеварительную панкреатическую секрецию, скоординированную с гастроинтестинальной моторикой. Межпищеварительное постпрандиальное выделение ПП и мотилина не соотносилось с наличием HP-инфекции, в то время как постпрандиальная и межпищеварительная секреция гастрина была выше у HP-позитивных больных. Межпищеварительная панкреатическая секреция амилазы, липазы и химотрипсина была достоверно выше у HP-позитивных лиц, в то время как постпрандиальная панкреатическая секреция ферментов имела лишь тенденцию к повышению. Гипергастринемия с ХК-подобными эффектами и альтернативное за-кисление двенадцатиперстной кишки [249] посредством гиперсекреции секретина могли способствовать межпищеварительной панкреатической гиперсекреции, в то время как оба фактора играли менее важную физиологическую роль в постпрандиальной стимуляции ПЖ. Исследование J. E. Dominguez-Munoz и P. Malfertheiner [184] также подтверждает предположение, что HP-инфекция у лиц с бессимптомным носительством связана с изменениями не только в физиологии желудочной секреции, но также и в секреции ПЖ, и что эта связь между ПЖ и HP теоретически может иметь патофизиологическое значение при заболеваниях pancreas. Helicobacter pylori и ХП.Существуют различные гипотезы о взаимодействии между HP и ПЖ у больных ХП. Первая — возможная роль HP в патогенезе и прогрессировании ХП, по крайней мере его идиопатических форм; вторая — влияние HP-инфекции на экзокринную панкреатическую секрецию у больных ХП с нарушением последней; третья — влияние самого ХП на гастроинтестинальную физиологию и потенцирование колонизации HP слизистой оболочки желудка [331]. Предположительная роль HP в патогенезе ХП высказана после исследований, показавших повреждение HP печеночной ткани в экспериментальных моделях на животных [214]. Недавние данные от J. G. Fox и соавт. 38 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
Приблизительно 10—30 % случаев панкреатитов могут быть определены как идиопатический ХП. Может ли данная бактериальная инфекция быть причиной по крайней мере части этих случаев, остается вопросом. В одном из последних исследований, проведенном в Италии [178], было оценено наличие ДНК-последовательности HP при помощи полимеразной цепной реакции в панкреатическом соке 40 пациентов с алкогольным ХП, инфицированных HP. В то время как все биопсии из желудка были НР-позитивные, ни в одном из случаев не было выявлено ДНК-последовательности HP в панкреатическом секрете. Авторы заключили, что антибактериальная активность панкреатического сока препятствует колонизации HP в ПЖ. Это исследование, однако, не изучало ДНК-последовательности других разновидностей рода Helicobacter и не дало определенного ответа на вопрос относительно того, может ли Helicobacter играть роль в патогенезе ХП в целом. Следует отметить, что G. Manes и соавт. у 40 больных ХП продемонстрировали отсутствие различий внешнесекреторной функции pancreas при всех морфологических стадиях болезни (по данным ЭРХПГ) между инфицированными и неинфицированными HP пациентами. Только тяжесть заболевания коррелировала с ухудшением функции pancreas у обследованных больных [332]. Интересны результаты исследований Л. А. Холоимовой и соавт., обследовавших 47 детей с хроническим дуоденитом и язвенной болезнью двенадцатиперстной кишки, ассоциированными с HP. Авторами отмечается, что в 98 % случаев имели место ультразвуковые признаки ХП (неоднородность паренхимы, диффузное повышение эхогенности ПЖ, нечеткость и неровность контуров железы), а в 91 % случаев имелись признаки внешнесекреторной недостаточности ПЖ (по данным микроскопии кала). При этом выраженность выявленных изменений морфологии и функции ПЖ не коррелировала со степенью воспалительных изменений слизистой оболочки двенадцатиперстной кишки [75]. По результатам исследований Л. Н. Малямовой (2003), несмотря на частую встречаемость ультразвуковых признаков ХП у детей с воспалительными и эрозивно-язвенными поражениями, ассоциированными с HP (62,7—73,8 %), признаки внешнесекреторной недостаточности ПЖ (стеа-торея) встречались достаточно редко [48]. Полученные данные далеко не однозначны, поскольку, во-первых, не совсем ясно, что явилось причиной изменений ПЖ — непосредственно HP, либо воспалительно-некротический процесс в двенадцатиперстной кишке, либо же совокупное воздействие этих и других факторов. Во-вторых, отсутствие признаков внешнесекреторной недостаточности ПЖ у детей, в большинстве случаев с коротким анамнезом заболевания, мало о чем говорит, поскольку возникновению экзокринной недостаточности ПЖ чаще предшествует длительный анамнез ХП. Некоторые исследователи определили увеличение как базальной, так и стимулированной желудочной кислотной секреции у HP-позитивных пациентов с ХП [397, 432], другие — гиперацидность в желудке посредством Глава 2. Этиология и патогенез хронического панкреатита • 39
G. Manes и соавт. [332] недавно изучили 40 пациентов с алкогольным ХП в сравнении с 40 здоровыми лицами и 40 больными с алкогольным циррозом печени без ХП с целью оценки распространенности НР-инфек-ции и характеристики слизистой оболочки желудка. Группа с алкогольным циррозом печени была специально введена для оценки потенциального риска токсического эффекта алкоголя на слизистую оболочку желудка. Авторами было определено, что распространенность HP-инфекции у больных ХП равна таковой у пациентов с алкогольным циррозом печени и у здоровых лиц (38 % при ХП, 30 % при циррозе печени и 28 % — у здоровых бессимптомных носителей). Авторы не нашли никаких различий активности и выраженности HP-ассоциированного гастрита. Наоборот, выраженность HP-негативного хронического гастрита в антральном отделе была достоверно выше у больных ХП по сравнению с группой больных циррозом печени и здоровыми HP-носителями. Это наблюдение приводит нас к гипотезе, что помимо алкоголя существуют другие факторы, вероятно, связанные с ХП, и потенцирующие развитие хронического НР-нега-тивного гастрита у больных ХП. В то же время, по данным Н. Б. Губергриц и И. Н. Остроуховой, частота обсемененности Helicobacter pylori у больных ХП составляет 86,5 %, причем у всех больных отмечены воспалительные или эрозивно-язвенные поражения гастродуоденальной зоны [14]. Конечно, существует вероятность, что данный факт связан с высокой инфицированностью HP в популяции России и Украины [27]. В этой связи нам хотелось бы обратиться к результатам другого исследования [362], в котором изучалась распространенность HP-инфекции у больных ХП с дуоденальными язвами и без таковых по сравнению с группой контроля, включавшей больных дуоденальной язвой без ХП. В этом исследовании 27 % больных ХП имели язву двенадцатиперстной кишки. Распространенность антител против HP (IgG) составила 22 % у больных ХП без язвы и 60 % в группе больных с сочетанной язвой двенадцатиперстной кишки и ХП. Для сравнения 86 % больных контрольной группы с дуоденальными язвами были инфицированы HP. Этот факт свидетельствует, что HP все-таки имеет какое-то значение в развитии дуоденальных язв у больных ХП, однако HP, скорее всего, это не единственная причина. Определенное патогенетическое значение здесь могут иметь нарушения микроциркуляции в слизистой оболочке желудка, изменения биохимии желчи и др. Helicobacter pylori и ОП.Возможная роль HP в развитии ОП до сих пор не изучена. В целом HP вряд ли является непосредственной причиной ОП, даже при так называемом идиопатическом ОП, однако нельзя полностью исключить влияния HP на развитие болезни. Усиленная стимуляция ПЖ в результате гипергастринемии или дуоденальной ацидификации, так же как перемещение HP или его токсинов из гастродуоденальной слизистой оболочки в ПЖ, являются потенциальными механизмами, объясняющими 40 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
С практической и клинической точек зрения, данные о взаимосвязи HP и панкреатита все еще недостаточны, чтобы подтвердить факт негативного влияния HP на течение заболеваний ПЖ. Однако нельзя не учитывать результаты клинических исследований, доказавших усугубление клиники ХП у больных, инфицированных HP, и определенный результат антихелико-бактерной терапии [13, 29, 362]. Так, по нашим данным, введение эради-кационной терапии в комплексную схему лечения обострения ХП у больных, инфицированных HP, приводило к достоверно более быстрому купированию болевого абдоминального синдрома и уменьшало средние сроки пребывания больного в стационаре. При динамическом наблюдении отмечен противорецидивный эффект эрадикационной терапии в отношении целого ряда случаев ХП [29]. В заключение следует отметить, что к настоящему моменту теоретически обоснована взаимосвязь HP-инфекции с заболеваниями ПЖ. Единичные эпидемиологические исследования не позволяют к настоящему моменту однозначно оценить масштаб данной взаимосвязи в различных регионах мира. Результаты проведенных в России клинических исследований, показавшие ранние и поздние эффекты тройной антихеликобактер-ной терапии у больных ХП, весьма обнадеживают, но требуют дальнейших исследований в этой области, пролонгированного мониторинга за обследованными больными [38]. 2.2.3. Наследственный панкреатит 2.2.3.1. Наследственный панкреатит с аутосомно-доминантным типом наследования Наследственный панкреатит (НП) с аутосомно-доминантным типом наследования впервые был описан М. V. Comfort и A. G. Streinberg в 1952 г. [159]. В дальнейшем было определено, что НП представляет собой патологию, с одинаковой частотой встречающуюся у лиц обоего пола [44, 387] и не имеющую расовой вариабельности. Он наиболее распространен в Северной Европе, его частота составляет 1—3 % из всех случаев ХП, однако данные о встречаемости НП постоянно увеличиваются в связи с усовершенствованием методов диагностики [388]. Так, частота НП за последние три десятилетия возросла более чем в 4 раза; по последним данным, его доля составляет около 5 % из всех этиологических форм панкреатитов [505]. С середины 1990-х годов несколько независимых групп начали использование революционных технологий молекулярной генетики для генетических исследований в области НП. Итоговым результатом явилось обнаружение D. Whitcomb и L. Bodic в 1996 г. мутации в 3-м экзоне гена катио-
Таким образом, к 1996 г. наследственным панкреатитом (inherited pancreatitis, hereditary pancreatitis) стало принято называть патологию ПЖ, наследуемую по аутосомно-доминантному типу с неполной пенетрантностью (80 %), морфологическим субстратом которой является воспаление ПЖ; клинически характеризующуюся повторными эпизодами ОП в виде болевого абдоминального и диспепсического синдромов, постепенно увеличивающейся частотой и выраженностью рецидивов, нарастанием степени функциональной (экзокринной и/или эндокринной) недостаточности, отягощенным семейным анамнезом, высоким риском рака ПЖ [44, 264, 286, 393]. Несмотря на то что НП впервые описан в 1952 г., этиология и патогенез НП до конца не изучены. С 1996 г., безусловно, доминирующей стала теория патогенеза, связывающая развитие НП с наследованием мутации гена катионического трипсиногена R117H. Эта мутация становится причиной устойчивости трипсиногена к гидролизу, неконтролируемой каскадной самоактивации трипсина с последующей активацией трипсином других панкреатических проферментов и аутолизом ткани ПЖ.
Таким образом, трипсиноген в физиологических условиях способен в незначительных количествах аутоактивироваться в ткани ПЖ и в основной Глава 2. Этиология и патогенез хронического панкреатита • 43
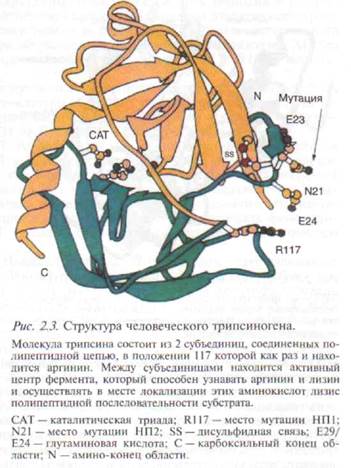
Существуют многочисленные дублирующие механизмы, препятствующие преждевременной активации трипсиногена и других проэнзимов в тканях ПЖ и ауто-лизу последней. К ним относятся [421]: 1) образование 2) разделение в 3) локализация 4) низкая концен 5) секреция панкреатического ингибитора трипсина (ПИТ); 6) способность ферментов ПЖ к аутолизу; 7) продукция а,-антитрипсина и (32-микроглобулина в печени, связы Молекула трипсина состоит из 2 субъединиц, соединенных полипептидной цепью, в положении 117 которой как раз и находится аргинин (рис. 2.3). Между субъединицами находится активный центр фермента, который способен узнавать аргинин и лизин и осуществлять в месте локализации этих аминокислот лизис полипептидной последовательности субстрата. Именно поэтому трипсин и трипсиноподобные ферменты (мезо-трипсин и энзим Y) способны инактивировать интрапанкреатические трипсиноген и трипсин, разрушая в положении аргинин-117 полипептидную цепь последних и обеспечивая до 80 % их инактивации [422]. Одним из основных механизмов, препятствующих в норме повреждению ПЖ, является панкреатический секреторный ингибитор трипсина (ПИТ) (рис. 2.4). ПИТ представляет собой специфический субстрат для 44 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
ПИТ, за счет ингиби-рования трипсина, предотвращает его последующую аутоакти-вацию и активацию других проэнзимов, однако количество трипсиногена значительно больше, чем ПИТ. Поэтому в период интенсивной активации трипсиногена ПИТ не может выполнять свою защитную роль. В этих обстоятельствах трипсин и трипсиноподобные ферменты, как было сказано ранее, возвращаются в цепь гидролиза, объединяющую две шаровидные области трипсина в R117, что вызывает длительную инактивацию трипсина и остановку каскада [207]. При мутации R117 и замене аргинина на гистидин в положении 117 трипсин и трипсиноподобные ферменты оказываются неспособными ли-зировать молекулы трипсиногена и трипсина, делая единственно возможным механизмом инактивации — ПИТ. У больных НП ПИТ продолжает функционировать в обычном режиме, однако мощности блокирующего эффекта ПИТ оказывается явно недостаточно и при воздействии какого-либо провоцирующего фактора (например, алкоголя) может произойти чрезмерная активация трипсиногена в трипсин, который не может быть инактивирован. Продолжается каскадная неконтролируемая активация панкреатических ферментов и аутодеструкция ПЖ, что в клиническом плане проявляется симптомокомплексом обострения ХП [44]. При этом для развития обострения НП достаточно, чтобы около 50 % молекул трипсиногена и трипсина были устойчивы к гидролизу [147]. Следует отметить, что при обследовании 21 пациента с хроническим алкогольным панкреатитом не было выявлено ни одного случая наличия мутаций R122H (R117H) или N291 (N211) [465]. Механизм, посредством которого мутация N211 приводит к развитию НП, не совсем ясен. Предполагается, что мутация N211 способствует ауто-активации трипсиногена, нарушая взаимодействие с ПИТ [234], либо препятствует инактивации трипсина, изменяя доступность начального участка гидролиза трипсина [143]. Высказывается предположение, что обе общих мутации, R117H и N211, не являются непосредственной причиной НП, а просто служат маркерами Глава 2. Этиология и патогенез хронического панкреатита • 45
Начиная с открытия мутации гена катионического трипсиногена, была предложена новая номенклатурная система для человеческих мутаций генома. Согласно последней была произведена замена терминов вышеуказанных мутаций с R117H на R122H и с N211 на N291 [91]. В исследованиях S. Т. Amann и L. К. Gates (2001) изучались экспрессия и пенетрация гена НП у монозиготных близнецов. Полученные данные свидетельствуют о том, что факторы окружающей среды вносят значимый вклад в степень пенетрации НП и, соответственно, в выраженность симптоматики и возраст начала заболевания. Становится понятно, что изучение механизма пенетрации в будущем поможет предотвращать фенотипи-ческое выражение НП у людей с генетической предрасположенностью [87].
В то же время, по результатам исследований V. Keim и соавт., проводивших обследование членов 30 семей больных ХП неясной этиологии (всего 550 человек), получены несколько другие данные. Так, в 6 семьях (25 человек) были выявлены мутации N291, а в 21 семье (76 человек) — мутации R122H, при этом большинство обследованных больных имели бессимптомное, либо умеренно выраженное течение — 26 и 42 % обследованных лиц соответственно. Тяжесть ХП и время манифестации клинической симптоматики заболевания не зависели от вида конкретной мутации [289]. P. Matew и соавт. показали, что в пределах семейства с НП болезнь развивается у лиц, имеющих более низкие уровни витамина Е и селена в сыворотке крови, и высокий уровень активности супероксидмутазы [337].
НП характеризуется ранним началом, часто поздним установлением диагноза, образованием кальцификатов, развитием экзокринной и эндокринной недостаточности, частым образованием псевдокист, развитием тромбозов воротной, селезеночной и нижней полой вен, геморрагии. Через 8— 10 лет у 20 % больных присоединяется сахарный диабет, у 15—20 % — выраженная стеаторея [329, 383]. Однако есть данные, опубликованные в 2003 г., показывающие, что темпы прогрессирования ХП, в том числе кальцификация, фиброз ПЖ и эндокринная недостаточность, быстрее и чаще развиваются у лиц с алкогольным ХП без наличия мутаций гена ка-тионического трипсиногена, чем у больных НП [291] (рис. 2.5). Выявленная зависимость может быть объяснена следующими положениями. Начальные признаки ХП более тщательно регистрируются у детей и подростков, страдающих НП, чем у больных алкогольным ХП, которые регулярно выпадают из поля зрения врачей, продолжая злоупотреблять алкоголем, и обращаются за медицинской помощью от случая к случаю только по поводу рецидивирующей абдоминальной боли. Зачастую впервые признаки алкогольного ХП регистрируются только при первичном обращении в стационар, что не всегда характеризует время начала болезни. Кроме того, прогрессирование заболевания с развитием эндокринной недостаточности может быть ускорено, поскольку более чем 50 % пациентов с алкогольным ХП продолжают злоупотреблять алкоголем после установления диагноза. Известно, что главным образом эндокринная ткань ПЖ чувствительна к воздействию алкоголя и при длительном периоде воздержания от приема алкоголя происходит некоторое восстановление секреторной способности ПЖ в отношении инсулина [245, 309]. Наконец, большинство лиц, злоупотребляющих алкоголем, являются курильщиками, что, как нами было показано ранее, также оказывает негативное воздействие на ПЖ, потенцируя развитие и прогрессирование ХП [272, 321]. С учетом совокупности проанализированных данных становится понятно, почему ав- Глава 2. Этиология и патогенез хронического панкреатита • 47
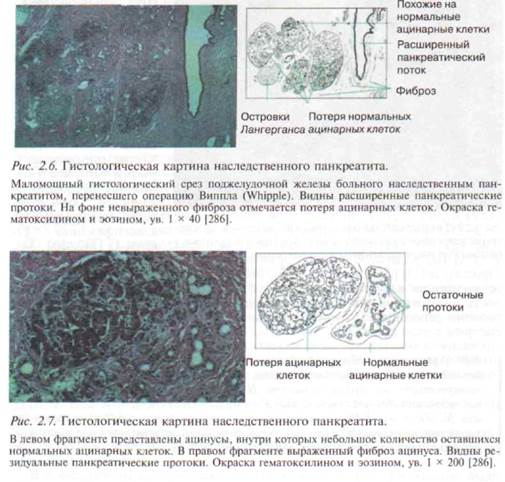
торами отмечена подобная зависимость, и алкогольный ХП, действительно, может протекать тяжелее, чем НП. При гистологическом исследовании наблюдаются патологические изменения, типичные и для других этиологических форм ХП [286, 448]. Типичными являются расширение панкреатических протоков, на фоне невыраженного фиброза отмечается атрофия ацинарных клеток, на поздней стадии заболевания возможна потеря островков Лангерганса (рис. 2.6, 2.7), в подавляющем большинстве случаев выявляются панкреатолитиаз и каль-цификация ПЖ [159, 505] (рис. 2.8). Заподозрить наследственную форму панкреатита позволяют отсутствие этиологических факторов и случаи панкреатита в семье у родственников больного. Действительно, у больных ХП без семейного анамнеза мутации N291 и R122H встречаются крайне редко [290]. Это является принципиальным для установления диагноза так называемого идиопатического ХП у пациентов без надежного семейного анамнеза [167], о чем будет сказано ниже. Существует мнение, что в развитии НП имеют значения мутации, принципиально другие, нежели те, о которых мы говорили выше, в частности мутации генов трансмембранного регулятора кистозного фиброза и 48 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
NB! С учетом международной номенклатуры, опираясь на проведенные за последние годы исследования, здесь и далее термином «наследственный панкреатит» мы будем называть НП с аутосомно-доминантным типом наследования без уточнения типа мутаций (R117H, или R122H, и N211, или N291), а для НП с аутосомно-рецессивным типом мы будем уточнять характер выявленных мутаций, что позволит читателям облегчить восприятие изложенного материала (примеч. авт.). 2.2.3.2. Наследственный панкреатит с аутосомно-рецессивным типом наследования В соответствии с вышеизложенным, преждевременная активация трипси-ногена в пределах ПЖ ведет к развитию ХП. При активации трипсиногена возможна каскадная активация многих других панкреатических проферментов с развитием аутолиза ПЖ. Кроме того, трипсин активирует аци-нарные клетки посредством стимуляции рецепторов к трипсину, которые, как стало недавно известно, являются одними из так называемых протеа-зактивированных рецепторов (тип 2). В результате такого механизма наблюдается избыточная экспрессия ацинарными и протоковыми клетками протеазактивированных рецепторов [264].
Глава 2. Этиология и патогенез хронического панкреатита • 49
Проведенные исследования идентифицировали варианты мутаций в гене ПИТ у больных ХП; с наибольшей частотой была обнаружена мутация N34S в 3-м экзоне гена ПИТ. Следует отметить, что мутация N34S была выделена совместно с двумя интронными мутациями: IVS1-37T>C и IVS3-69INSTTTT, причем аналогичный набор мутаций (N34S + IVS1-37T>C + IVS3-69insTTTT) наблюдался в различных странах мира [146, 189, 264, 393, 473, 509]. Мутация N34S была выявлена у 20—23 % больных с НП [278], у больных идиопатическим ХП [393, 509], алкогольным ХП [111] и тропическим кальцифицирующим |



 Существует мнение, что развитие ХП у части пациентов, принимающих алкоголь в дозе менее 50 г/сут в течение 2 лет, позволяет предполагать наличие других этиологических факторов (курение, очень низкое или высокое потребление жира и белка с пищей) в патогенезе заболевания [43]. В то же время существует мнение, что недоедание, а также тип алкогольного напитка не оказывают существенного влияния на заболеваемость ХП [429].
Существует мнение, что развитие ХП у части пациентов, принимающих алкоголь в дозе менее 50 г/сут в течение 2 лет, позволяет предполагать наличие других этиологических факторов (курение, очень низкое или высокое потребление жира и белка с пищей) в патогенезе заболевания [43]. В то же время существует мнение, что недоедание, а также тип алкогольного напитка не оказывают существенного влияния на заболеваемость ХП [429].
 30 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ
30 • ХРОНИЧЕСКИЙ ПАНКРЕАТИТ му повышению базального давления в протоке ПЖ, что затрудняло отток панкреатического секрета [313].
му повышению базального давления в протоке ПЖ, что затрудняло отток панкреатического секрета [313]. В опытах in vitro показано, что алкоголь, по-видимому, за счет нарушения баланса между протеазами и их ингибиторами в соке ПЖ, стимулирует секрецию активированных ферментов. Предполагается, что в панкреатическом секрете у лиц, злоупотребляющих алкоголем, повышено отношение трипсиногена к ингибиторам трипсина, что предрасполагает к внутри-протоковой активации ферментов [74]. К настоящему моменту имеются только экспериментальные данные, доказывающие снижение активности ингибитора трипсина на фоне приема алкоголя у крыс [445].
В опытах in vitro показано, что алкоголь, по-видимому, за счет нарушения баланса между протеазами и их ингибиторами в соке ПЖ, стимулирует секрецию активированных ферментов. Предполагается, что в панкреатическом секрете у лиц, злоупотребляющих алкоголем, повышено отношение трипсиногена к ингибиторам трипсина, что предрасполагает к внутри-протоковой активации ферментов [74]. К настоящему моменту имеются только экспериментальные данные, доказывающие снижение активности ингибитора трипсина на фоне приема алкоголя у крыс [445].
 назвали токсичной [37], а В. А. Тарасов и соавт.— «агрессивной» [68]. Именно проникновение в панкреатический проток такой желчи и является патологическим механизмом, поддерживающим воспалительный процесс в ПЖ, и основной причиной развития хронического билиарного панкреатита. Однако точные механизмы, активирующие ферменты в клетках ацину-сов при обструкции, до сих пор не известны [74]. Существует предположение [49], что при холелитиазе желчь содержит значительные количества продуктов перекисного окисления липидов, что и придает ей особые агрессивные свойства при рефлюксе в панкреатические протоки.
назвали токсичной [37], а В. А. Тарасов и соавт.— «агрессивной» [68]. Именно проникновение в панкреатический проток такой желчи и является патологическим механизмом, поддерживающим воспалительный процесс в ПЖ, и основной причиной развития хронического билиарного панкреатита. Однако точные механизмы, активирующие ферменты в клетках ацину-сов при обструкции, до сих пор не известны [74]. Существует предположение [49], что при холелитиазе желчь содержит значительные количества продуктов перекисного окисления липидов, что и придает ей особые агрессивные свойства при рефлюксе в панкреатические протоки. верхнебрыжеечными сосудами — артериомезентериальная непроходимость, лимфаденит в области связки Трейтца, синдром приводящей петли после резекции желудка и др.) [45].
верхнебрыжеечными сосудами — артериомезентериальная непроходимость, лимфаденит в области связки Трейтца, синдром приводящей петли после резекции желудка и др.) [45]. ной болезнью двенадцатиперстной кишки является гиперацидность в желудке с чрезмерной стимуляцией ПЖ соляной кислотой посредством гиперпродукции секретина. Это приводит к секреторному напряжению ПЖ в условиях затруднения оттока, а следовательно, к внутрипротоковой гипер-тензии.
ной болезнью двенадцатиперстной кишки является гиперацидность в желудке с чрезмерной стимуляцией ПЖ соляной кислотой посредством гиперпродукции секретина. Это приводит к секреторному напряжению ПЖ в условиях затруднения оттока, а следовательно, к внутрипротоковой гипер-тензии. ли дозозависимое снижение секреции амилазы при введении вакуолизи-рующего токсина HP.
ли дозозависимое снижение секреции амилазы при введении вакуолизи-рующего токсина HP. [215] также демонстрируют присутствие одной из разновидностей рода Helicobacter в желчи и тканях желчного пузыря больных хроническим холециститом. Н. J. Monstein и соавт. идентифицировали HP в желчных камнях у больных хроническим калькулезным холециститом [350], который, как мы сообщали ранее, является одной из причин развития билиарноза-висимого ХП. В недавнем отечественном исследовании HP был выявлен в конкрементах желчного пузыря у 18,8 % больных [57].
[215] также демонстрируют присутствие одной из разновидностей рода Helicobacter в желчи и тканях желчного пузыря больных хроническим холециститом. Н. J. Monstein и соавт. идентифицировали HP в желчных камнях у больных хроническим калькулезным холециститом [350], который, как мы сообщали ранее, является одной из причин развития билиарноза-висимого ХП. В недавнем отечественном исследовании HP был выявлен в конкрементах желчного пузыря у 18,8 % больных [57]. суточного мониторирования рН у больных ХП с внешнесекреторной недостаточностью ПЖ [123, 380]. Однако существуют данные и об уменьшении постпрандиальной секреции кислоты с гипергастринемией у больных ХП [409]. Следует отметить, что все эти исследования не учитывали эндоскопические и гистологические особенности слизистой оболочки желудка, знание которых могло бы помочь в интерпретации противоречивых данных. Изменения функции желудка, описанные у больных ХП, скорее могли отражать присутствие HP-инфекции в его слизистой оболочке, чем изменения, вызванные патологией ПЖ.
суточного мониторирования рН у больных ХП с внешнесекреторной недостаточностью ПЖ [123, 380]. Однако существуют данные и об уменьшении постпрандиальной секреции кислоты с гипергастринемией у больных ХП [409]. Следует отметить, что все эти исследования не учитывали эндоскопические и гистологические особенности слизистой оболочки желудка, знание которых могло бы помочь в интерпретации противоречивых данных. Изменения функции желудка, описанные у больных ХП, скорее могли отражать присутствие HP-инфекции в его слизистой оболочке, чем изменения, вызванные патологией ПЖ. возможное влияние HP на развитие ОП [331]. Z. Warzecha и соавт. изучали эффект HP-инфекции слизистой оболочки желудка на модели ишемиче-ского ОП. При наличии HP-инфекции было отмечено существенное сокращение притока крови и усиление ишемического повреждения в ПЖ после реперфузии. Плазменные уровни амилазы, липазы, так же как IL-ip и IL-10, были достоверно выше у инфицированных животных. Авторы интерпретировали эти данные как свидетельство негативного эффекта НР-инфекции в желудке на течение ОП. Это могло быть связано и с выделением бактериями липополисахаридов, что приводило к активации лейкоцитов и усилению местной и общей воспалительной реакции [501].
возможное влияние HP на развитие ОП [331]. Z. Warzecha и соавт. изучали эффект HP-инфекции слизистой оболочки желудка на модели ишемиче-ского ОП. При наличии HP-инфекции было отмечено существенное сокращение притока крови и усиление ишемического повреждения в ПЖ после реперфузии. Плазменные уровни амилазы, липазы, так же как IL-ip и IL-10, были достоверно выше у инфицированных животных. Авторы интерпретировали эти данные как свидетельство негативного эффекта НР-инфекции в желудке на течение ОП. Это могло быть связано и с выделением бактериями липополисахаридов, что приводило к активации лейкоцитов и усилению местной и общей воспалительной реакции [501]. Глава 2. Этиология и патогенез хронического панкреатита • 41
Глава 2. Этиология и патогенез хронического панкреатита • 41
 нического трипсиногена (PRSSl-гене) длинного .плеча 7-й хромосомы (7q35) [316, 504, 505]. Было установлено, что транзиция гуанина на аденин с изменением кодонов (CGC -> САС) приводит к замене аргинина на гистидин в положении 117 (Rl 17H) аминокислотной последовательности фермента (рис. 2.1). Вторая мутация в PRSSl-гене была впоследствии обнаружена во 2-м экзоне —N211 [234]. Эти две мутации (R117H и N211) к настоящему времени идентифицированы в семействах с НП во многих странах, включая Францию [210], Германию [464], Великобританию [168], Японию [365, 367] и США [234, 505].
нического трипсиногена (PRSSl-гене) длинного .плеча 7-й хромосомы (7q35) [316, 504, 505]. Было установлено, что транзиция гуанина на аденин с изменением кодонов (CGC -> САС) приводит к замене аргинина на гистидин в положении 117 (Rl 17H) аминокислотной последовательности фермента (рис. 2.1). Вторая мутация в PRSSl-гене была впоследствии обнаружена во 2-м экзоне —N211 [234]. Эти две мутации (R117H и N211) к настоящему времени идентифицированы в семействах с НП во многих странах, включая Францию [210], Германию [464], Великобританию [168], Японию [365, 367] и США [234, 505]. В условиях здоровой ПЖ фракция трипсиногена аутоактивируется в трипсин (рис. 2.2). Выявленная транзиция принципиально меняет всю систему регуляции интрапанкреатической активации зимогенов. Известно,
В условиях здоровой ПЖ фракция трипсиногена аутоактивируется в трипсин (рис. 2.2). Выявленная транзиция принципиально меняет всю систему регуляции интрапанкреатической активации зимогенов. Известно,







 трипсина, необратимо
трипсина, необратимо множества связанных панкреатогенных дефектов, хотя авторами и признается тот факт, что несоответствующее предотвращение дезактивации трипсина в пределах ПЖ ответственно за развитие НП в большинстве случаев [143]. В то же время при обследовании более чем 800 пациентов с ХП без семейного анамнеза было выявлено, что мутации N291 и R122H встречаются очень редко [290].
множества связанных панкреатогенных дефектов, хотя авторами и признается тот факт, что несоответствующее предотвращение дезактивации трипсина в пределах ПЖ ответственно за развитие НП в большинстве случаев [143]. В то же время при обследовании более чем 800 пациентов с ХП без семейного анамнеза было выявлено, что мутации N291 и R122H встречаются очень редко [290]. В Великобритании (Ньюкасл) наблюдаются пациенты, принадлежащие к 13 семействам с НП. Данные относительно 9 из этих семейств были ранее опубликованы [168]. R122H (R117H) мутация была идентифицирована в 3 семействах, а мутация N291 (N211) демонстрировалась в 5. В контрольной группе не выявлено ни одной из вышеуказанных мутаций в любом из пяти экзонов гена PRSS1. Авторами было произведено сравнение различных характеристик между группами с различными мутациями. Средний возраст манифестации НП был более высоким в R122H группе (8,4 против 6,5 года, р = 0,007), большее количество пациентов с R122H-MyTa4Heft характеризовалось развернутой клинической картиной к 20-летнему возрасту (89 % против 64 %). Большее количество пациентов с R122H мутацией требовало хирургического вмешательства (8 из 12 против 4 из 17, р = 0,029), причем оперативное пособие в этой группе было выполнено в более раннем возрасте. Отмечена также тенденция у большинства пациентов с мутацией R122H к развитию экзокринной недостаточности ПЖ, однако тяжесть диабета и возраст его манифестации в обеих группах достоверно не различались. В обеих группах алкоголь одинаково провоцировал обострение заболевания. Эти наблюдения были также отмечены при первоначальном описании мутации N211 в 1997 г. [234] и также были отмечены в European Registry of Hereditary Pancreatitis and Pancreatic Cancer (EUROPAC) [267]. Данные о том, что у пациентов с мутацией R122H заболевание манифестирует в более раннем возрасте и чаще возникает необходимость в хирургическом лечении, встречаются и в других источниках [436].
В Великобритании (Ньюкасл) наблюдаются пациенты, принадлежащие к 13 семействам с НП. Данные относительно 9 из этих семейств были ранее опубликованы [168]. R122H (R117H) мутация была идентифицирована в 3 семействах, а мутация N291 (N211) демонстрировалась в 5. В контрольной группе не выявлено ни одной из вышеуказанных мутаций в любом из пяти экзонов гена PRSS1. Авторами было произведено сравнение различных характеристик между группами с различными мутациями. Средний возраст манифестации НП был более высоким в R122H группе (8,4 против 6,5 года, р = 0,007), большее количество пациентов с R122H-MyTa4Heft характеризовалось развернутой клинической картиной к 20-летнему возрасту (89 % против 64 %). Большее количество пациентов с R122H мутацией требовало хирургического вмешательства (8 из 12 против 4 из 17, р = 0,029), причем оперативное пособие в этой группе было выполнено в более раннем возрасте. Отмечена также тенденция у большинства пациентов с мутацией R122H к развитию экзокринной недостаточности ПЖ, однако тяжесть диабета и возраст его манифестации в обеих группах достоверно не различались. В обеих группах алкоголь одинаково провоцировал обострение заболевания. Эти наблюдения были также отмечены при первоначальном описании мутации N211 в 1997 г. [234] и также были отмечены в European Registry of Hereditary Pancreatitis and Pancreatic Cancer (EUROPAC) [267]. Данные о том, что у пациентов с мутацией R122H заболевание манифестирует в более раннем возрасте и чаще возникает необходимость в хирургическом лечении, встречаются и в других источниках [436].


 Активность трипсина в поджелудочной железе главным образом управляется ПИТ, который также известен как serine protease inhibitor Kazal тип 1 (SPINKJ). ПИТ синтезируется в ацинарных клетках ПЖ и действует как мощный естественный ингибитор трипсина, предотвращая аутолиз ПЖ и, следовательно, развитие ХП. ПИТ также блокирует дальнейшую активацию выделения ферментов панкреатическими клетками посредством инги-бирования протеазактивированных рецепторов [264].
Активность трипсина в поджелудочной железе главным образом управляется ПИТ, который также известен как serine protease inhibitor Kazal тип 1 (SPINKJ). ПИТ синтезируется в ацинарных клетках ПЖ и действует как мощный естественный ингибитор трипсина, предотвращая аутолиз ПЖ и, следовательно, развитие ХП. ПИТ также блокирует дальнейшую активацию выделения ферментов панкреатическими клетками посредством инги-бирования протеазактивированных рецепторов [264]. Впоследствии была предложена гипотеза, заключающаяся в том, что если генетическая мутация ПИТ нарушает его функцию, то трипсин может легко вызывать аутолиз ПЖ с развитием острого или хронического панкреатита. Было предположено, что мутация гена ПИТ может вызывать предрасположенность к развитию ХП, понижая функцию блокирования активации трипсина. Пять независимых групп на основании начатых одновременно исследований сообщили о наличии у пациентов с ХП мутаций гена ПИТ, расположенного на 5-й хромосоме [146, 282, 304, 375, 393, 509]. Проведенными в дальнейшем исследованиями действительно было доказано, что мутации в гене ПИТ связаны с развитием ХП [111, 145, 189, 372, 510]. Однако значение и особенности наследования мутаций гена ПИТ не одинаково интерпретируются различными группами исследователей.
Впоследствии была предложена гипотеза, заключающаяся в том, что если генетическая мутация ПИТ нарушает его функцию, то трипсин может легко вызывать аутолиз ПЖ с развитием острого или хронического панкреатита. Было предположено, что мутация гена ПИТ может вызывать предрасположенность к развитию ХП, понижая функцию блокирования активации трипсина. Пять независимых групп на основании начатых одновременно исследований сообщили о наличии у пациентов с ХП мутаций гена ПИТ, расположенного на 5-й хромосоме [146, 282, 304, 375, 393, 509]. Проведенными в дальнейшем исследованиями действительно было доказано, что мутации в гене ПИТ связаны с развитием ХП [111, 145, 189, 372, 510]. Однако значение и особенности наследования мутаций гена ПИТ не одинаково интерпретируются различными группами исследователей.