 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Элементы молекулярно-кинетической (МКТ) и квантовой теории теплоемкости
Молекулярно-кинетическая теория
В соответствии с МКТ при хаотическом движении учитывается только поступательное и вращательное движение молекул, а остальными видами движения пренебрегают. Пространственное движение молекул раскладывается вдоль осей х, y, z. Считается, что внутренняя энергия равномерно распределяется вдоль х, у, z. В зависимости от количества атомов в молекуле число степеней свободы составляет I ат. газ (Ar) - i = 3 II ат. газ (N2) - i = 5 III и более ат. газ (СО2) - i = 6 Покажем связь между с, u, R, μR, Т. После преобразования уравнения для расчета давления по МКТ, записанного для 1 м3.
Легко получить, что
откуда
Считают, что внутренняя энергия и распределяется равномерно по осям. Тогда для (i = 1) уравнение принимает вид:
Для любого числа степеней свободы это уравнение принимает вид: - для 1 кмоля
-для 1 кг
Установим связь между с, i и R для двух процессов: изохорного и изобарного. Изохорный процесс: Так как по первому закону термодинамики в изохорном процессе
В зависимости от атомности газов μсv составляют I ат. газ (Ar): i = 3, II ат. газ (N2): i = 5, III ат. газ (СО2): i = 6, Тогда, например, для воздуха:
Изобарный процесс: Из уравнения Майера получим:
Например, для воздуха: Тогда для разных газов будем иметь I ат. газ (Ar): i = 3, II ат. газ (N2): i = 5, III ат. газ (CO2) i = 6, Следовательно, при одной и той же атомности газов μcv и μcp для разных газов - величины постоянные. Например, для воздуха:
Теплоемкость идеальных газов зависит только от молекулярной массы, температуры и характера процесса Теплоемкость реальных газов зависит также и от давления.
Показатель адиабаты и его зависимость от температуры
Показателем адиабаты является относительная теплоемкость
Выразим показатель адиабаты через число степеней свободы
С учетом уравнения Майера формула принимает вид
Из уравнения видно, что при R = const с увеличением температуры cv увеличивается, следовательно, показатель адиабаты k уменьшается.
Теплоемкость газовых смесей Для газовых смесей массовая, объемная и мольная теплоемкости составляют:
Например, для воздуха:
Элементы квантовой теории теплоемкости Недостаток МКТ - эта теория учитывает только поступательное и вращательное движение молекул и не учитывает колебательные движения атомов в молекуле. В соответствии с квантовой теорией теплоемкости энергия колебания атомов в молекулах учитывается, причем колебательная частота ω определяется опытным путем по спектроскопическим исследованием газа. Колебания считают гармоническими. Тогда, например, мольная теплоемкость газов в идеальном состоянии может быть подсчитана по формуле:
n - число вращательных степеней свободы; для двухатомных и многоатомных газов n = 2;
h = 6,62 · 10-34 Дж/с - постоянная Планка; k = 1,38 · 10-23 Дж/К - постоянная Больцмана; v ,1/с - частота колебаний; μR, Дж/(кмоль · К) - универсальная газовая постоянная.
Лабораторная установка Лабораторная установка состоит из калориметрической трубки 1, которая заключена в стеклянной оболочке 2. В трубке 1 расположена электрическая спираль 3. Воздух просасывается с помощью вентилятора 4, а его расход определяется с помощью газового счетчика 5. Температура воздуха на входе t1 и выходе t2 из нагревательной системы фиксируется с помощью термометров 6, 7. Мощность электроспирали 3 регулируется реостатом 8, а измеряется вольтметром 9.
Рис. Схема лабораторной установки
Порядок проведения работы 3.1. Перед началом работы необходимо заполнить таблицу 1. Таблица 1 - Характеристика измерительных приборов
3.2. Регулятором 8 установить минимальную мощность электронагревателя (примерного 50 Вт). 3.3. При достижении стационарного режима определить расход воздуха, проходящего через трубку калориметра 1. 3.4. Записать показания приборов в таблицу 2. Таблица 2 - Параметры, которые измеряются
|



 .
. ,
, .
. .
. кДж/(кг · К);
кДж/(кг · К); кДж/(кг · К)
кДж/(кг · К) , при
, при  ,
,  , то
, то ,
,  .
. кДж/(кг · К)
кДж/(кг · К) кДж/(кг · К)
кДж/(кг · К)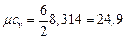 кДж/(кг · К)
кДж/(кг · К) кДж/(кг · К)
кДж/(кг · К) ,
, ;
;  .
. кДж/(кг · К)
кДж/(кг · К) кДж/(кмоль · К)
кДж/(кмоль · К) кДж/(кмоль · К)
кДж/(кмоль · К) кДж/(кмоль · К)
кДж/(кмоль · К) кДж/(кг · К)
кДж/(кг · К) .
. ;
; .
. кДж/(кг · К);
кДж/(кг · К);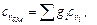 кДж/(кг · К);
кДж/(кг · К); кДж/(м3 · К);
кДж/(м3 · К);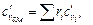 кДж/(м3 · К);
кДж/(м3 · К); кДж/(кмоль · К);
кДж/(кмоль · К); кДж/(кмоль · К).
кДж/(кмоль · К).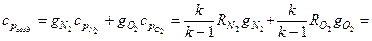
 Дж/(кг · К).
Дж/(кг · К). .
. , k - характеристическая температура (имеется в таблицах);
, k - характеристическая температура (имеется в таблицах);
