ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Организация структуры молекулы белка. Цветные реакции белков.
Состоят из 4 структур: Первичная структура(цепочка)-это последовательность расположения аминокислотных остатков в полипептидной цепи. Аминокислоты соединяются в полипептид с помощью ковалентных (амидных) связей. Вторичная структура (спираль)- это упорядоченное строение полипептидных цепей, обусловленное водородными связями между группами С=О и N-H разных аминокислот. Третичная структура (глобула, шар)- большинство белков имеют весьма компактную структуру, которая определяется формой, размером и полярностью аминокислотных радикалов, а также последовательностью аминокислот. Четвертичная структура (соединение нескольких молекул третичной структуры в сложный комплекс)- взаимное расположение нескольких полипептидных цепей в составе единого белкового комплекса. Белковые молекулы, входящие в состав белка с четвертичной структурой, образуются на рибосомах по отдельности и лишь после окончания синтеза образуют общую надмолекулярную структуру. Цветные реакции
· Ксантопротеиновая–происходит взаимодействие ароматических и гетероатомных циклов в молекуле белка с концентрированной азотной кислотой, сопровождаю- щеееся появлением желтой окраски; · Биуретовая – происходит взаимодействие слабощелочных растворов белков с раствором сульфата меди(II) с образованием комплексных соединений между ионами Cu2+ и полипептидами. Реакция сопровождается появлением фиолетово–синей окраски; · при нагревании белков со щелочью в присутствии солей свинца выпадает черный осадок, который содержит серу. Белки: биологическое значение классификация, физические свойства.
Белки– это биополимеры, состоящие из остатков α-аминокислот, соединённых между собой пептидными связями (-CO-NH-). Белки входят в состав клеток и тканей всех живых организмов. В молекулы белков входит 20 остатков различных аминокислот.
Физические свойства Свойства белков весьма разнообразны, которые они выполняют. Одни белки растворяются в воде, образуя, как правило, коллоидные растворы (например, белок яйца); другие растворяются в разбавленных растворах солей; третьи нерастворимы (например, белки покровных тканей). Химические свойства Денатурация – разрушение вторичной, третичной структуры белка под действием различных факторов: температура, действие кислот, солей тяжёлых металлов, спиртов и т.д. При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и других факторов) происходит измене- ние вторичной, третичной и четвертичной структур белковой макромолекулы, то есть ее нативной пространственной структуры. Первичная структура, а следователь- но, и химический состав белка не меняются. Изменяются физические свойства: сни- жается растворимость, способность к гидратации, теряется биологическая актив-ность. Меняется форма белковой макромолекулы, происходит агрегирование. В то же время увеличивается активность некоторых групп, облегчается воздействие на белки протеолитических ферментов, а, следовательно, он легче гидролизуется. В пищевой технологии особое практическое значение имеет тепловая денатура- ция белков, степень которой зависит от температуры, продолжительности нагрева и влажности. Это необходимо помнить при разработке режимов термообработке пи- щевого сырья,полуфабрикатов, а иногда и готовых продуктов. Особую роль про- цессы тепловой денатурации играют при бланшировании растительного сырья, суш- ке зерна, выпечке хлеба, получении макаронных изделий. Денатурация белков может вызываться и механическим воздействием (давлением, растиранием, встряхиванием, ультразвуком). К денатурации белков приводит действие химических реагентов (кислот, щелочей, спирта, ацетона). Все эти приемы широко используют в пищевой и биотехнологии.
Качественные реакции на белки: а) При горении белка – запах палёных перьев. б) Белок +HNO3 → жёлтая окраска в) Раствор белка +NaOH + CuSO4 → фиолетовая окраска
Гидролиз Белок + Н2О → смесь аминокислот Функции белков в природе: · каталитические (ферменты); · регуляторные (гормоны); · структурные (кератин шерсти, фиброин шелка, коллаген); · двигательные (актин, миозин); · транспортные (гемоглобин); · запасные (казеин, яичный альбумин); · защитные (иммуноглобулины) и т.д. Гидратация Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объем увеличивается. Набухание бел- ка сопровождается его частичным растворением. Гидрофильность отдельных белков зависит от их строения. Имеющиеся в составе и расположенные на поверхности бел- ковой макромолекулы гидрофильные амидные (–CO–NH–, пептидная связь), амин- ные (NH2) и карбоксильные (COOH) группы притягивают к себе молекулы воды, строго ориентируя их на поверхность молекулы. Окружая белковые глобулы гидрат- ная (водная) оболочка препятствует устойчивости растворов белка. В изоэлектричес- кой точке белки обладают наименьшей способностью связывать воду, происходит разрушение гидратной оболочки вокруг белковых молекул, поэтому они соединяют- ся, образуя крупные агрегаты. Агрегация белковых молекул происходит и при их обезвоживании с помощью некоторых органических растворителей, например этило- вого спирта. Это приводит к выпадению белков в осадок. При изменении pH среды макромолекула белка становится заряженной, и его гидратационная способность ме- няется. При ограниченном набухании концентрированные белковые растворы образуют сложные системы, называемые студнями. Студни не текучи, упруги, обладают плас-тичностью, определенной механической прочностью, способны сохранять свою фор- му. Глобулярные белки могут полностью гидратироваться, растворяясь в воде (нап- ример, белки молока), образуя растворы с невысокой концентрацией. Гидрофильные свойства белков имеют большое значение в биологии и пищевой промышленности. Очень подвижным студнем, построенным в основном из молекул белка, является цитоплазма– полужидкое содержимое клетки. Сильно гидратированный студень–сырая клейковина, выделенная из пшеничного теста, она содержит до 65% воды. Гидрофильность, главное качество зерна пшеницы, белков зерна и муки играет боль- шую роль при хранении и переработке зерна, в хлебопечении. Тесто, которое полу- чают в хлебопекарном производстве, представляет собой набухший в воде белок, концентрированный студень, содержащий зерна крахмала. Пенообразование Процесс пенообразования–это способность белков образовывать высококонцент- рированные системы «жидкость–газ»,называемые пенами. Устойчивость пены, в ко- торой белок является пенообразователем, зависит не только от его природы и от кон- цнтрации,но и от температуры. Белки в качестве пенообразователей широко используются в кондитерской промышленности (пастила, зефир, суфле). Структуру пены имеет хлеб, а это влияет на его вкусовые свойства. Горение Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев. Аминокислоты.
Аминокислотами называются азотосодержащие органические вещества, молекулы которых содержат карбоксильную группу – COOH и аминогруппу – NH2.
NH2 –CH2 –COOH NH2 –CH2 –CH2 –COOH аминоуксусная кислота β-аминопропиновая кислота CH3-CH-COOH α-аминопропиновая кислота
Физические свойства Аминокислоты – бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом. Химические свойства 1. Кислотные свойства а) Взаимодействие со щелочами NH2 –CH2 –COOH + NaOH →NH2 –CH2 –COONa + H2O б) Взаимодействие со спиртами NH2 –CH2 –COOH + C2H5OH →NH2 –CH2 –COOC2H5 + H2O
2. Основные свойства Взаимодействие с кислотами NH2 –CH2 –COOH + HCl → NH3Cl–CH2 –COOH Аминокислоты – амфотерные вещества.
3. Аминокислоты взаимодействуют друг с другом
NH2 –CH2 –COOH + NH2 –CH2 –COOH → NH2 –CH2 –CO-NH–CH2 –COOH + Н2О дипептид -СО–NH – пептидная группа (амидная группа) Применение Аминокислоты, преимущественно α-аминокислоты, необходимы для синтеза белков в живых организмах. Нужные для этого аминокислоты человек и животные получают в виде пищи, содержащей различные белки. Последние подвергаются в пищеварительном тракте расщеплению на отдельные аминокислоты, из которых затем синтезируются белки, свойственные данному организму. Некоторые аминокислоты применяются в медицинских целях. Многие аминокислоты служат для подкормки животных. Производные аминокислот используются для синтеза волокна, например капрона.
Целлюлоза (клетчатка)
Целлюлоза (C 6 H 10 O 5 ) n – природный полимер, полисахарид, состоящий из остатков β-глюкозы, молекулы имеют линейное строение. В каждом остатке молекулы глюкозы содержатся три гидроксильные группы, поэтому она проявляет свойства многоатомного спирта.
Физические свойства Целлюлоза – волокнистое вещество, нерастворимое ни в воде, ни в обычных органических растворителях, гигроскопична. Обладает большой механической и химической прочностью. 1. Целлюлоза, или клетчатка, входит в состав растений, образуя в них оболочки клеток. 2. Отсюда происходит и ее название (от лат. «целлула» – клетка). 3. Целлюлоза придает растениям необходимую прочность и эластичность и является как бы их скелетом. 4. Волокна хлопка содержат до 98 % целлюлозы. 5. Волокна льна и конопли также в основном состоят из целлюлозы; в древесине она составляет около 50 %. 6. Бумага, хлопчатобумажные ткани – это изделия из целлюлозы. 7. Особенно чистыми образцами целлюлозы являются вата, полученная из очищенного хлопка, и фильтровальная (непроклеенная) бумага. 8. Выделенная из природных материалов целлюлоза представляет собой твердое волокнистое вещество, не растворяющееся ни в воде, ни в обычных органических растворителях.
Химические свойства 1. Целлюлоза – полисахирид, подвергается гидролизу с образованием глюкозы: (C6H10O5)n + nН2О → nС6Н12О6 2. Целлюлоза – многоатомный спирт, вступает в реакции этерификации с образованием сложных эфиров (С6Н7О2(ОН)3)n + 3nCH3COOH → 3nH2O + (С6Н7О2(ОCOCH3)3)n триацетат целлюлозы Ацетаты целлюлозы – искусственные полимеры, применяются в производстве ацетатного шёлка, плёнки (киноплёнки), лаков. Применение Применение целлюлозы весьма разнообразно. Из неё получают бумагу, ткани, лаки, плёнки, взрывчатые вещества, искусственный шёлк (ацетатный, вискозный), пластмассы (целлулоид), глюкозу и многое другое. Нахождение целлюлозы в природе. 1. В природных волоконцах макромолекулы целлюлозы располагаются в одном направлении: они ориентированы вдоль оси волокна. 2. Возникающие при этом многочисленные водородные связи между гидроксильными группами макромолекул обусловливают высокую прочность этих волокон. 3. В процессе прядения хлопка, льна и т. д. эти элементарные волокна сплетаются в более длинные нити. 4. Это объясняется тем, что макромолекулы в ней хотя и имеют линейную структуру, но расположены более беспорядочно, не ориентированы в одном направлении. Построение макромолекул крахмала и целлюлозы из разных циклических форм глюкозы существенно сказывается на их свойствах: 1) крахмал является важным продуктом питания человека, целлюлоза для этой цели использоваться не может; 2) причина состоит в том, что ферменты, способствующие гидролизу крахмала, не действуют на связи между остатками целлюлозы.
Углеводы Углеводами называют природные органические соединения, имеющие, как правило, общую формулу СmН2nОn(Сm(Н2O )n), где т и n і 3.Исключение составляют дезоксисахара, которые имеют общую формулу СmН2п+2On. В зависимости от способности к гидролизу все углеводы делятся на: моносахариды — углеводы, молекулы которых не подвержены гидролизу; дисахариды— углеводы, из молекул которых при гидролизе образуется от двух до десяти одинаковых или различных моносахаридов; полисахариды — углеводы, из молекул которых при гидролизе образуется от десятков тысяч и выше одинаковых или различных моносахаридов. Углеводы — распространенный в природе класс органических соединений. В растениях углеводы образуются в результате реакции фотосинтеза из CO2 и Н2О:
Крахмал
Целлюлоза (C 6 H 10 O 5 ) n – природный полимер, полисахарид, состоящий из остатков β-глюкозы, молекулы имеют линейное строение. В каждом остатке молекулы глюкозы содержатся три гидроксильные группы, поэтому она проявляет свойства многоатомного спирта. Физические свойства Целлюлоза – волокнистое вещество, нерастворимое ни в воде, ни в обычных органических растворителях, гигроскопична. Обладает большой механической и химической прочностью. 1. Целлюлоза, или клетчатка, входит в состав растений, образуя в них оболочки клеток. 2. Отсюда происходит и ее название (от лат. «целлула» – клетка). 3. Целлюлоза придает растениям необходимую прочность и эластичность и является как бы их скелетом. 4. Волокна хлопка содержат до 98 % целлюлозы. 5. Волокна льна и конопли также в основном состоят из целлюлозы; в древесине она составляет около 50 %. 6. Бумага, хлопчатобумажные ткани – это изделия из целлюлозы. 7. Особенно чистыми образцами целлюлозы являются вата, полученная из очищенного хлопка, и фильтровальная (непроклеенная) бумага. 8. Выделенная из природных материалов целлюлоза представляет собой твердое волокнистое вещество, не растворяющееся ни в воде, ни в обычных органических растворителях. Химические свойства 1. Целлюлоза – полисахирид, подвергается гидролизу с образованием глюкозы: (C6H10O5)n + nН2О → nС6Н12О6 2. Целлюлоза – многоатомный спирт, вступает в реакции этерификации с образованием сложных эфиров (С6Н7О2(ОН)3)n + 3nCH3COOH → 3nH2O + (С6Н7О2(ОCOCH3)3)n триацетат целлюлозы Ацетаты целлюлозы – искусственные полимеры, применяются в производстве ацетатного шёлка, плёнки (киноплёнки), лаков. Применение Применение целлюлозы весьма разнообразно. Из неё получают бумагу, ткани, лаки, плёнки, взрывчатые вещества, искусственный шёлк (ацетатный, вискозный), пластмассы (целлулоид), глюкозу и многое другое. Нахождение целлюлозы в природе. 1. В природных волоконцах макромолекулы целлюлозы располагаются в одном направлении: они ориентированы вдоль оси волокна. 2. Возникающие при этом многочисленные водородные связи между гидроксильными группами макромолекул обусловливают высокую прочность этих волокон. 3. В процессе прядения хлопка, льна и т. д. эти элементарные волокна сплетаются в более длинные нити. Построение макромолекул крахмала и целлюлозы из разных циклических форм глюкозы существенно сказывается на их свойствах: 1) крахмал является важным продуктом питания человека, целлюлоза для этой цели использоваться не может; 2) причина состоит в том, что ферменты, способствующие гидролизу крахмала, не действуют на связи между остатками целлюлозы.
Дисахариды
К широко распространенным и имеющим важное значение как компоненты пищевых продуктов, относятся дисахариды: сахароза, лактоза, мальтоза и др. По химическому строению дисахариды являются гликозидами моносахаридов. Большинство дисахаридов состоят из гексоз, но в природе известны дисахариды, состоящие из одной молекулы гексозы и одной молекулы пентозы. При образовании дисахарида одна молекула моносахарида всегда образует связь со второй молекулой с помощью своего полуацетального гидроксила. Другая молекула моносахарида может соединяться либо также полуацетальным гидрокислом, либо одним из спиртовых гидроксилов. В последнем случае в молекуле дисахарида будет оставаться свободным один полуацетальный гидроксил. Мальтоза – резервный олигосахарид – обнаружена во многих растениях в небольших количествах, в больших количествах накапливается в солоде – обычно в семенах ячменя, проросших в определенных условиях. Поэтому мальтозу часто называют солодовым сахаром. Мальтоза образуется в растительных и животных организмах в результате гидролиза крахмала под действием амилаз. Мальтоза содержит два остатка Д-глюкопиранозы, соединенных между собой a(1®4)гликозидной связью.
Мальтоза обладает восстанавливающими свойствами, что используется при ее количественном определении. Она легко растворима в воде. Раствор обнаруживает мутаротацию. Под действием фермента a-глюкозидазы (мальтазы) солодовый сахар гидролизуется с образованием двух молекул глюкозы:
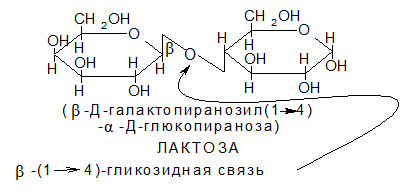
Мальтоза сбраживается дрожжами. Эта способность мальтозы используется в технологии бродильных производств при производстве пива, спирта этилового и т.д. из крахмалсодержащего сырья. Лактоза – резервный дисахарид (молочный сахар) – содержится в молоке (4-5%) и получается в сыроваренной промышленности из молочной сыворотки после отделения творога. Сбраживается лишь особыми лактозными дрожжами, содержащимися в кефире и кумысе. Лактоза построена из остатков b-Д-галактопиранозы и a-Д-глюкопиранозы, соединенных между собой b-(1→4)-гликозидной связью. Лактоза является восстанавливающим дисахаридом, причем свободный полуацетальный гидроксил принадлежит остатку глюкозы, а кислородный мостик связывает первый углеродный атом остатка галактозы с четвертым атомом углерода остатка глюкозы.
Лактоза гидролизуется под действием фермента b-галактозидазы (лактазы):
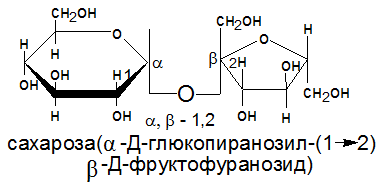
Лактоза отличается от других сахаров отсутствием гигроскопичности – она не отсыревает. Молочный сахар применяется как фармацевтический препарат и как питательное средство для грудных детей. Водные растворы лактозы мутаротируют, лактоза имеет в 4-5 раз менее сладкий вкус, чем сахароза. Содержание лактозы в женском молоке достигает 8%. Из женского молока выделено более 10 олигосахаридов, структурным фрагментом которых служит лактоза. Эти олигосахариды имеют большое значение для формирования кишечной флоры новорожденных, некоторые из них подавляют рост болезнетворных кишечных бактерий, в частности – лактулоза. Сахароза (тростниковый сахар, свекловичный сахар) – это резервный дисахарид – чрезвычайно широко распространена в растениях, особенно много ее в корнеплодах свеклы (от 14 до 20%), а также в стеблях сахарного тростника (от 14 до 25%). Сахароза является транспортным сахаром, в виде которого углерод и энергия транспортируются по растению. Именно в виде сахарозы углеводы перемещаются из мест синтеза (листья) к месту, где они откладываются в запас (плоды, корнеплоды, семена). Сахароза состоит из a-Д-глюкопиранозы и b-Д-фруктофуранозы, соединенных a-1→b-2-связью за счет гликозидных гидроксилов:
Сахароза не содержит свободного полуацетального гидроксила, поэтому она не способна к окси-оксо-таутомерии и является невосстанавливающим дисахаридом. При нагревании с кислотами или под действием ферментов a-глюкозидазы и b-фруктофуранозидазы (инвертазы) сахароза гидролизуется с образованием смеси равных количеств глюкозы и фруктозы, которая называется инвертным сахаром.
|