 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Дослід 4. Визначення вмісту йонів Кадмію в питній воді комплексонометричним методом
ЛАБОРАТОРНИЙ ПРАКТИКУМ «ВПЛИВ ЗАБРУДНЕННЯ ДОВКІЛЛЯ НА ОРГАНІЗМ ЛЮДИНИ» Дослід 1. Дослідження консервних банок на домішки свинцю Проводять у витяжній шафі! Прилади та обладнання: вата. Реактиви: ацетон, 40%-ний розчин етанової кислоти, 4%-ний розчин калій йодиду. Очищають для дослідження поверхню банки від жиру шматочком вати, змоченої ацетоном. Інший шматочок вати змочують 40%-ним розчином етанової кислоти і накладають на 3-4 хв на очищене місце. Потім на те ж місце накладають шматочок вати, змоченої 4%-ним розчином калій йодиду. Швидке пожовтіння вати внаслідок утворення плюмбум (ІІ) йодиду вказує на домішку Плюмбуму вище за норму, тобто більше 1% (допускається не більше 0,04%).
Дослід 2. Визначення вмісту нітрат-іонів у рослинах Прилади та обладнання: предметне скло, скальпель, піпетка. Реактиви: 1%-ний розчин дифеніламіну. На предметне скло помістити декілька зрізів різних частин рослин. На кожен зріз нанесіть по одній краплі 1% розчину дифеніламіну. Спостерігайте за появою синього забарвлення. Інтенсивність забарвлення порівняєте з таблицею.
Дослід 3. Визначення нітратів у питній воді Присутність нітратів у природних водах пов'язано з внутрішньоводними процесами нітрифікації амонійних іонів, які відбуваються в присутності кисню під дією нітрифікуючих бактерій: NH4+ + OH‾ + 3/2O2 = H+ + NO2‾ + 2H2O NO2‾ + 1/2O2 = NO3‾ Збільшення концентрації нітрат-іонів спостерігається тому в літній час в період масового відмирання фітопланктону і високою активності нітрифікаторів. Іншим важливим джерелом збагачення поверхневих вод нітратами є утворюється при атмосферних електричних розрядах оксидів Нітрогену, які після поглинання атмосферними водами потрапляють на земну поверхню. Вміст нітратів в атмосферних опадах досягає нерідко 1 мг N/л. Велика кількість нітратів може надходити в водні об'єкти з промисловими і господарсько-побутовими стічними водами особливо після їх біологічної очистки. Крім того, нітрати потрапляють в поверхневі води зі стоком з сільгоспугідь і зі стоками води зі зрошуваних полів, на яких застосовуються азотні добрива. Підвищений вміст нітратів вказує на погіршення становища водного об'єкта. ГДК нітрат-іонів = 40 мг/л. Принцип визначення нітратів колориметричним методом з дифеніламіном заснований на колориметруванні забарвлених продуктів реакції, які утворюються при взаємодії дифениламина з нітрат іонами в сильно кислому середовищі. При цьому дифениламин окиснюється нітратною кислотою і утворюється хіноїдна амонієва сіль діфенілбензідіна, забарвлена в інтенсивно синій колір. У пробірку наливають 1 мл аналізованої води, додають 1 краплю розчину NaCl і обережно по стінках пробірки, уникаючи перемішування, доливають декілька крапель розчину дифениламина в сульфатній кислоті. У присутності нітратів на кордоні дотику розчинів утворюється блакитне кільце, швидкість появи якого і інтенсивність забарвлення залежать від вмісту нітратів. Приблизну кількість нітратів можна визначити за даними табл. Таблиця Вміст нітрат-іонів
Дослід 4. Визначення вмісту йонів Кадмію в питній воді комплексонометричним методом Обладнання: конічна колба на 250 мл; бюретка для титрування; піпетки на 10 мл, бюкс для зважування, аналітичні терези Реактиви: аміачний буферний розчин; 0,1 н розчин трилону Б; індикатор хромоген чорний ЕТ-00 (еріохром чорний). Метод застосовується в тому випадку, якщо вміст Купруму в стічній воді не перевищує 20 мкг/л, так як більш висока концентрація цього елементу перешкоджає точності визначення вмісту Кадмію. 100 мл досліджуваної води поміщають в конічну колбу ємністю 250 мл, наливають в колбу 10 мл буферного розчину (54 г амоній хлориду і 350 мл 25% розчину аміаку в 1 л дистильованої води), додають 0,2 г індикатора хромогену чорного ЕТ-00 і титрують 0,1 н розчином трилону Б до переходу винно-червоного забарвлення в синє. Вміст Кадмію в г/л обчислюють за формулою: Х = Т – титр 0,1 н розчину трилону Б по Кадмію, теоретично він дорівнює 0,00562 г/мл; V – кількість 0,1 н трилону Б, витраченого на титрування в мл; VВ – кількість стічної води, взятої для аналізу, мл.
|



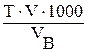 , де
, де