 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение
Как определить диапазон голоса - ваш вокал
Игровые автоматы с быстрым выводом
Как цель узнает о ваших желаниях прежде, чем вы начнете действовать. Как компании прогнозируют привычки и манипулируют ими
Целительная привычка
Как самому избавиться от обидчивости
Противоречивые взгляды на качества, присущие мужчинам
Тренинг уверенности в себе
Вкуснейший "Салат из свеклы с чесноком"
Натюрморт и его изобразительные возможности
Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д.
Как научиться брать на себя ответственность
Зачем нужны границы в отношениях с детьми?
Световозвращающие элементы на детской одежде
Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия
Как слышать голос Бога
Классификация ожирения по ИМТ (ВОЗ)
Глава 3. Завет мужчины с женщиной

Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
 Отёска стен и прирубка косяков - Когда на доме не достаёт окон и дверей, красивое высокое крыльцо ещё только в воображении, приходится подниматься с улицы в дом по трапу. Отёска стен и прирубка косяков - Когда на доме не достаёт окон и дверей, красивое высокое крыльцо ещё только в воображении, приходится подниматься с улицы в дом по трапу.
 Дифференциальные уравнения второго порядка (модель рынка с прогнозируемыми ценами) - В простых моделях рынка спрос и предложение обычно полагают зависящими только от текущей цены на товар. Дифференциальные уравнения второго порядка (модель рынка с прогнозируемыми ценами) - В простых моделях рынка спрос и предложение обычно полагают зависящими только от текущей цены на товар.
| Одержання алотропних модифікацій Оксигену та Сульфуру.
Неорганічна хімія Неметали Якщо в Періодичній системі умовно провести лінію по діагоналі від Бора до Астату, то праворуч угорі в головних підгрупах будуть розташованіелементи-неметали. До них належать: Гідроген, Гелій, Бор, Карбон, Нітроген, Оксиген, Флуор, Неон, Силіцій, Фосфор, Сульфур, Хлор, Аргон, Арсен, Селен, Бром, Криптон, Телур, Йод, Ксенон, Астат, Радон. Оксиген, Сульфур. Алотропні модифікації. Сполуки оксигену та сульфуру Оксиген, Сульфур ЕлементОксигенрозташований в 2-му періоді, VI групі Періодичної системи. Порядковий номер — 8, відносна атомна маса — 16.
Електронна конфігурація атома Оксигену:


В атомі Оксигену два неспарені електрони, отже, він двовалентний. В Оксигену висока електронегативність, тому в сполуках для нього характерний ступінь окиснення –2, крім сполук із Флуором (ступінь окиснення +1 і +2) і пероксидів (ступінь окиснення –1).
ЕлементСульфуррозташований в 3-му періоді, VI групі Періодичної системи. Порядковий номер — 16. Відносна атомна маса — 32.
Електронна конфігурація атома Сульфуру:


З урахуванням можливості переходу електронів з s- та p- підрівнів на вільний d-підрівень для Сульфуру в сполуках характерні ступені окиснення –2, +4, +6, рідше +2.
Алотропні модифікації Оксигену. У вільному стані Оксиген утворює дві алотропні модифікації: кисень  і озон і озон  . .
Властивості алотропних модифікацій Оксигену

Алотропні модифікації Сульфуру. При кімнатній температурі Сульфур перебуває у вигляді  -сірки (ромбічна модифікація), що являє собою жовті крихткі кристали без запаху, нерозчинні у воді. За температур вище -сірки (ромбічна модифікація), що являє собою жовті крихткі кристали без запаху, нерозчинні у воді. За температур вище  відбувається повільне перетворення відбувається повільне перетворення  -сірки в -сірки в  -сірку (моноклінна модифікація), що є майже білими кристалічними пластинками. -сірку (моноклінна модифікація), що є майже білими кристалічними пластинками.
Поширення Оксигену в природі. Оксиген — найпоширеніший елемент на Землі. Його вміст у земній корі складає близько 55,1 %. Оксиген як хімічний елемент входить до складу води, мінералів (відомо понад 1400 мінералів, що містять Оксиген), органічних речовин.
Поширення Сульфуру в природі. У природі Сульфур зустрічається у вигляді самородної сірки (проста речовина); входить до складу сульфідів і сульфатів, що утворюють багато мінералів, є компонентом природного вугілля та нафти. Сульфур — життєво важливий елемент: він входить до складу білків. Одержання алотропних модифікацій Оксигену та Сульфуру. 1) Кисень утворюється в результаті розкладання деяких солей:

пероксидів: 
оксидів важких металів: 
2) Озон утворюється зі звичайного кисню під дією електричного розряду (розряд блискавки, робота електротрансформаторів) або ультрафіолетового випромінювання (сонячне світло, робота ксерокса), а також у процесах, що супроводжуються виділення атомарного Оксигену (розклад пероксидів).
3) Сірку добувають в самородному стані; також її добувають:
при неповному розкладанні сірководню:

із сульфідів металів:

в реакціях відновлення сірки із сульфур(IV) оксиду:


Хімічні властивості кисню.
Кисень — сильний окисник.
1) Взаємодія з металами:

2) Взаємодія з неметалами:
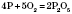
3) Горіння складних речовин:

4) Окиснення складних речовин (цей процес не належить до горіння):

Хімічні властивості сірки.
1) При взаємодії з неметалами сірка виявляє окисні й відновлювальні властивості.
Із простими речовинами, утвореними більш електронегативними елементами (Оксигеном, Фтором, Хлором, Бромом), сірка виступає в ролі відновника.
 — сульфур(IV) оксид — сульфур(IV) оксид
Із простими речовинами, утвореними менш електронегативними елементами, сірка виступає в ролі окисника:
 — карбон(VI) сульфід — карбон(VI) сульфід
Бінарні сполуки сульфуру, в яких вона виявляє ступінь окиснення –2, називаютьсульфідами.
 — гідроген сульфід (сірководень) — гідроген сульфід (сірководень)
2) Взаємодія з металами.
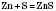 — цинк сульфід; — цинк сульфід;
 — ферум(ІІ) сульфід. — ферум(ІІ) сульфід.
Усі сульфіди, крім HgS, утворюються при нагріванні. Із ртуттю сірка взаємодіє вже при кімнатній температурі:
 — меркурій(II) сульфід. — меркурій(II) сульфід.
Ця властивість використовується в лабораторіях для видалення розлитої ртуті, пари якої дуже токсичні.
Застосування кисню. Кисень використовується для інтенсифікації процесів горіння (наприклад, при виплавці сталі), підвищення температури горіння (при зварюванні), як окисник в інших реакціях, у медицині.
Озон має дезинфікуючу відбілюючу дію. Головне застосування озону — знезаражування водопровідної води.
Застосування сірки. Сірка застосовується для одержання сульфатної кислоти, вулканізації каучуку, боротьби із сільськогосподарськими шкідниками, одержання сірників, пороху. У медицині виготовляють сірчані мазі для лікування шкірних хвороб. Сульфур оксиди Сульфур(IV) оксид  (діоксид сірки, сірчистий газ, сірчистий ангідрид) — безбарвний газ із різким запахом, скраплюється при (діоксид сірки, сірчистий газ, сірчистий ангідрид) — безбарвний газ із різким запахом, скраплюється при  . Негорючий, легко розчиняється у воді. Водний розчин . Негорючий, легко розчиняється у воді. Водний розчин  називають сульфідною кислотою. називають сульфідною кислотою.
Міститься у вулканічних газах, виділяється при спалюванні природного вугілля. Є одним з основних забруднювачів повітря, викликає кислотні дощі.
Отруйний, викликає кашель, задишку, бронхіт, запалення легень.
Одержання сульфур(IV) оксиду.
1) Випалювання мінералів, що містять сульфіди:


2) Горіння сірки на повітрі: 
3) Горіння сірководню в надлишку кисню:  . .
4) Взаємодія міді з концентрованою сульфатною кислотою:

5) Дія сульфатної кислоти на сульфіти:

Хімічні властивості сульфур(IV) оксиду. Для  більш характерні відновлювальні властивості. більш характерні відновлювальні властивості.
1) Реакції, що відбуваються без зміни ступеня окиснення.
Взаємодія з основами:

Оборотна взаємодія з водою:
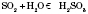
Взаємодія з основними оксидами:
 . .
2) Реакції, що відбуваються з підвищенням ступеня окиснення від +4 до +6, наприклад:

3) Реакції, що проходять зі зниженням ступеня окиснення, наприклад:

Застосування сульфур(IV) оксиду. Основна маса сульфур(IV) оксиду витрачається на виробництво сульфатної кислоти та інших сполук Сульфуру. Використовується для відбілювання паперу, соломи і вовни. На відміну від необоротної дії білильного вапна, знебарвлення сульфур(IV) оксидом часто оборотне, і забарвлення повертається після промивання. Використовується як дезінфікуючий засіб, наприклад для обробки підвалів, овочесховищ.
Сульфур(VI) оксид  (сірчаний газ, ангідрид сульфатної кислоти) при кімнатній температурі — безбарвна рідина, температура кипіння (сірчаний газ, ангідрид сульфатної кислоти) при кімнатній температурі — безбарвна рідина, температура кипіння  . Негорючий. Добре розчиняється у воді, взаємодіючи з нею. Гігроскопічний. . Негорючий. Добре розчиняється у воді, взаємодіючи з нею. Гігроскопічний.
Токсичний, уражає дихальні шляхи, викликає опіки шкіри.
Одержання сульфур(VI) оксиду. Окиснювання  в присутності каталізатора (платина чи ванадій(V) оксид) при високому тиску й нагріванні: в присутності каталізатора (платина чи ванадій(V) оксид) при високому тиску й нагріванні:

Хімічні властивості сульфур(VI) оксиду.
1) З’єднуючись із водою, утворює сульфатну кислоту:

2) Добре розчиняється в сульфатній кислоті, утворюючи важку маслянисту рідину — олеум:
 (або (або 
3) У температурному інтервалі від 400 до  розкладається на сульфур(IV) оксид і кисень: розкладається на сульфур(IV) оксид і кисень:

4) Як типовий кислотний оксид взаємодіє:
з оксидами, утвореними металами:

з основами:

Застосування сульфур(VI) оксиду. Сульфур(VI) оксид застосовується в основному у виробництві сульфатної кислоти; у лабораторії як водовід’ємний засіб. Сульфатна кислота Фізичні властивості сульфатної кислоти. Сульфатна кислота  — важка безбарвна масляниста рідина (стара назва сульфатної кислоти — купоросна олія). За звичайної температури вона не летка й не має запаху. — важка безбарвна масляниста рідина (стара назва сульфатної кислоти — купоросна олія). За звичайної температури вона не летка й не має запаху.
Одержання сульфатної кислоти. Найбільше значення маєконтактний спосібодержання сульфатної кислоти. Процес складається з трьох стадій.
1) Одержання сульфур(IV) оксиду. Сировиною є сульфурвмісні руди, сірка, сірководень:
 ; ;  ; ;  . .
2) Окиснення сульфур(IV) оксиду в сульфур(VI) оксид:  (реакція йде під тиском, при підвищеній температурі й у присутності каталізаторів). (реакція йде під тиском, при підвищеній температурі й у присутності каталізаторів).
3) Одержання сульфатної кислоти. При цьому сульфур(VI) оксид поглинають розведеною сульфатною кислотою, одержуючи олеум, який потім розбавляють до потрібної концентрації:  (або (або  ). ).
Хімічні властивості розведеної сульфатної кислоти. Сульфатна кислота як двоосновна кислота утворює два ряди солей: кислі —гідросульфати(утворюються при надлишку кислоти) і середні —сульфати.
1) Ступенева дисоціація:


2) Взаємодія з розчинними і нерозчинними основами (реакція нейтралізації). При цьому утворюються гідросульфати (якщо кислота в реакційній суміші в надлишку):

або сульфати (якщо немає надлишку кислоти в реакційній суміші):

3) Взаємодія з металами, що розташовані в електрохімічному ряді напруг до Гідрогену:

4) Взаємодія з оксидами металів:

5) Взаємодія із солями, утвореними більш слабкими і/або леткими кислотами:

Хімічні властивості концентрованої сульфатної кислоти.
1) Взаємодія з металами. Концентрована сульфатна кислота при нагріванні реагує з багатьма металами, у тому числі тими, що стоять в електрохімічному ряді напруг після Гідрогену. При цьому виділяється не водень, а сульфур(VI) оксид (з менш активними металами), сірка (з металами середньої активності) або сірководень (з активними металами):



Алюміній, залізо і хром пасивуються концентрованою сульфатною кислотою на холоді, при нагріванні реагують із нею.
2) Безводна сульфатна кислота розчиняє до 70 % сульфур(VI) оксиду, при цьому утворюється олеум.
3) При нагріванні відщеплює сульфур(VI) оксид доти, поки не утвориться розчин із масовою часткою сульфатної кислоти 98,3 %:

4) Обвуглює органічні речовини — цукор, папір, дерево.
5) Як сильна нелетка кислота витісняє інші кислоти з їхніх сухих солей:

Реактивом для виявлення сульфат-іонів є розчини, що містять йони Барію:

Барій сульфат, що утворюється,— білий порошкоподібний осад, нерозчинний у воді й кислотах.
Застосування сульфатної кислоти. Сульфатна кислота використовується у виробництві неорганічних кислот, лугів, солей, мінеральних добрив, вибухових речовин, штучних волокон, барвників, пластмас і багатьох інших речовин. Найбільша кількість її витрачається для одержання фосфатних і нітратних добрив. Сульфатну кислоту використовують для одержання інших кислот — хлоридної, флуороводневої, фосфатної, оцтової. Вона застосовується для очищення нафтопродуктів.
|








 і озон
і озон  .
.
 -сірки (ромбічна модифікація), що являє собою жовті крихткі кристали без запаху, нерозчинні у воді. За температур вище
-сірки (ромбічна модифікація), що являє собою жовті крихткі кристали без запаху, нерозчинні у воді. За температур вище  відбувається повільне перетворення
відбувається повільне перетворення  -сірку (моноклінна модифікація), що є майже білими кристалічними пластинками.
-сірку (моноклінна модифікація), що є майже білими кристалічними пластинками.







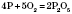


 — сульфур(IV) оксид
— сульфур(IV) оксид — карбон(VI) сульфід
— карбон(VI) сульфід — гідроген сульфід (сірководень)
— гідроген сульфід (сірководень)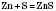 — цинк сульфід;
— цинк сульфід; — ферум(ІІ) сульфід.
— ферум(ІІ) сульфід. — меркурій(II) сульфід.
— меркурій(II) сульфід. (діоксид сірки, сірчистий газ, сірчистий ангідрид) — безбарвний газ із різким запахом, скраплюється при
(діоксид сірки, сірчистий газ, сірчистий ангідрид) — безбарвний газ із різким запахом, скраплюється при  . Негорючий, легко розчиняється у воді. Водний розчин
. Негорючий, легко розчиняється у воді. Водний розчин 

 .
.


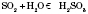
 .
.
 (сірчаний газ, ангідрид сульфатної кислоти) при кімнатній температурі — безбарвна рідина, температура кипіння
(сірчаний газ, ангідрид сульфатної кислоти) при кімнатній температурі — безбарвна рідина, температура кипіння  . Негорючий. Добре розчиняється у воді, взаємодіючи з нею. Гігроскопічний.
. Негорючий. Добре розчиняється у воді, взаємодіючи з нею. Гігроскопічний.

 (або
(або 
 розкладається на сульфур(IV) оксид і кисень:
розкладається на сульфур(IV) оксид і кисень:


 — важка безбарвна масляниста рідина (стара назва сульфатної кислоти — купоросна олія). За звичайної температури вона не летка й не має запаху.
— важка безбарвна масляниста рідина (стара назва сульфатної кислоти — купоросна олія). За звичайної температури вона не летка й не має запаху. ;
;  ;
;  .
. (або
(або  ).
).











