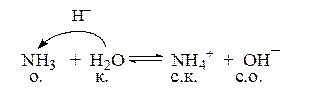ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Классификация кислот и оснований.
К занятию на неделе с 7 по 12 марта Протолитическая теория кислот и оснований. Классическое представление о кислотах и основаниях дает теория Аррениуса. Согласно этой теории: Кислота – электролит, при диссоциации которого образуется в качестве катиона – ион водорода. Основание – электролит, при диссоциации которого образуется в качестве аниона – гидроксид-ион. Однако, эта теория не может объяснить кислотно-основные свойства веществ, таких как аммиак, анилин – проявляющих основные свойства и галогенидов металлов или неметаллов (PCl5), проявляющих кислотные свойства. Поэтому в 1923 году Бренстедом и Лоури была предложена более общая теория кислот и оснований. Основные положения протолитической теории: 1. Кислотно-основные реакции осуществляются за счет переноса протона Н+ от кислоты к основанию. 2. Реакции, сопровождающиеся переносом Н+, называются протолитическими, а вещества, участвующие в них – протолитами. 3. Кислота – это протолит, который является донором Н+, т.е. способна отдавать протон. Кислота, отдавая протон, превращается в основание, которое называется сопряженным. Кислота ⇄ H+ + сопряженное основание HCl ⇄ H+ + Cl – кислота сопр. осн-е 4. Основание – это протолит, который является акцептором протона H+, т.е. способно принимать протон. Основание, присоединив H+, превращается в кислоту, которая называется сопряженной. Основание + H+ ⇄ сопряженная кислота NН3 + H+ ⇄ NH4+ основание сопр. к-та
5. Кислота и соответствующее ей сопряженное основание или основание и сопряженная с ним кислота образуют протолитические пары или сопряженные кислотно-основные пары: HCl - Cl – ; NН3 - NH4+ к с.о о. с.к. Сила кислоты определяется ее способностью отдавать H+, а сила основания – его способностью присоединять H+. Поэтому сильная кислота, отдав протон, превращается в слабое сопряженное основание, т.е. частицу, плохо присоединяющую протон, а сильное основание – соответственно, в слабую сопряженную кислоту.
В каждой протолитической реакции участвуют 2 пары кислот и оснований и схематически это можно изобразить так:
HCl/Cl-, H2O/H3O+
NH3/NH4+, H2O/H3O+
Классификация кислот и оснований. По теории Бренстеда и Лоури, как видно из примеров, понятия кислоты и основания значительно расширены. Кислотами и основаниями могут быть как молекулы, так и ионы. Примеры протолитов.
Из приведенных примеров видно, что есть вещества или частицы, способные проявлять свойства и кислот и оснований, например вода.
H2О ⇄ H+ + ОН – Н2О + H+ ⇄ H3О+ кислота сопр. осн-е основание сопр. к-та Протолиты, способные как отдавать протон, так и принимать протон, т.е. обладающие как протонодонорными, так и протоноакцепторными свойствами, называются амфолиты. К амфолитам относятся: вода, спирты, карбоновые кислоты, жидкий аммиак, гидрид анионы многоосновных кислот и т.д. Характерной реакцией амфолитов является реакция кислотно-основного диспропорционирования или автопротолиза (самоионизации).
|