 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Теория фотометрического метода
Метод анализа, основанный на переведении определяемого компонента в поглощающее свет соединение с последующим определением количества этого компонента путём измерения светопоглощения раствора полученного соединения, называется фотометрическим. По окраске растворов окрашенных веществ можно определять концентрацию того или иного компонента или визуально, или при помощи фотоэлементов – приборов, превращающих световую энергию в электрическую. В соответствии с этим различают фотометрический визуальный метод анализа, называемый часто колориметрическим, и метод анализа с применением фотоэлементов – собственно фотометрический метод анализа. Фотометрический метод является объективным методом, поскольку результаты его не зависят от способностей наблюдателя, в отличие от результатов колориметрического – субъективного метода. Фотометрический метод анализа – один из самых старых и распространённых методов физико-химического анализа. Его распространению способствовали сравнительная простота необходимого оборудования, особенно для визуальных методов, высокая чувствительность и возможность применения для определения почти всех элементов периодической системы и большого количества органических веществ. Открытие всё новых и новых реагентов, образующих окрашенные соединения с неорганическими ионами и органическими веществами, делает в настоящее время применение этого метода почти неограниченным. Фотометрический метод анализа может применяться для большого диапазона определяемых концентраций. Его используют как для определения основных компонентов различных сложных технических объектов с содержанием до 20 -30% определяемого компонента, так и для определения микропримесей в этих объектах при содержании их до 10-3 – 10-4 %. Комбинирование фотометрических методов с некоторыми методами разделения – хромотографическим, экстракционным позволяет на 1-2 порядка повысить чувствительность определения, доведя его до 10-5 . В некоторых случаях фотометрический метод может быть применён для одновременного определения в растворе в растворе нескольких ионов, хотя его возможности ограничены. Очень ценно использование фотометрических методов для решения многих теоретических вопросов аналитической и физической химии. Способность химического соединения, неорганического иона и органической группировки поглощать лучистую энергию определённых длин волн используется в фотометрическом анализе. Среди неорганических веществ сравнительно немного соединений, обладающих собственной окраской: это соединения марганца (VII), хрома (VI), меди (II) и др. Каждое вещество обладает способностью поглощать лучистую энергию в виде квантов энергии, соответствующих определённым длинам волн. Линии или полосы поглощения располагаются в ультрафиолетовой, видимой или инфракрасной областях спектра. Эти полосы и линии могут быть использованы для качественного и количественного фотометрического анализа. Основной закон фотометрии
Если световой поток интенсивности I0 падает на кювету, содержащую исследуемый раствор, то часть этого потока Iк отражается от стенок кюветы и поверхности раствора, часть его Iа поглощается молекулами вещества, содержащегося в растворе, и расходуется на изменение электронной, вращательной и колебательной энергии этих молекул, часть Iа1 поглощается молекулами самого растворителя. Если в растворе присутствуют твёрдые частицы в виде мутей или взвесей, то часть световой энергии Ir отражается и от этих частиц и, наконец, часть энергии It проходит через кювету. На основании закона сохранения энергии можно написать уравнение:
I0 = Iк + Iа + Iа1 + Ir + It (1)
При анализе прозрачных растворов в уравнении (1) член Ir равен 0. при работе на протяжении всего исследования с одним растворителем член Iа1 можно считать постоянным. Кроме того, растворители всегда подбирают так, чтобы они сами в исследуемой области спектра обладали минимальным поглощением, которым можно пренебречь. При использовании одной и той же кюветы значение отражённого светового потока Iк очень мало и им можно пренебречь. Поэтому уравнение (1) можно упростить:
I0 = Iа + It (2)
Непосредственными измерениями можно определить интенсивность падающего светового потока (I0) и прошедшего через анализируемый раствор (It). Значение Iа может быть найдено по разности между I0 и It ; непосредственному же измерению эта величина не поддаётся. На основании многочисленных экспериментов П. Бугером, а затем и И.Ламбертом был сформулирован закон, устанавливающий, что слои вещества одинаковой толщины, при прочих равных условиях, всегда поглощают одну и ту же часть падающего на них светового потока.
Закон Бугера-Ламберта
Два раствора одного и того же соединения различной концентрации одинаковы по оттенкам цвета, но различаются по интенсивности окраски. Интенсивность окраски измеряют по ослаблению энергии светового потока определённой длины волны. Интенсивность входящего светового потока обозначают обычно I0 , а интенсивность ослабленного поглощением светового потока через I. Величину поглощения света можно выражать разницей этих двух величин, или их отношением. Для различных фотометрических исследований наиболее удобно выражать интенсивность светопоглощения величиной:
Эта величина называется оптической плотностью и постоянно применяется в различных расчётах. Удобство применения именно этой функции обусловлено прямой пропорциональностью между оптической плотностью и концентрацией, а также толщиной слоя раствора окрашенного соединения. Рассмотрим поглощение света раствором вещества, находящегося в кювете с параллельными стенками. Толщину слоя поглощающего свет раствора обозначим через b, а интенсивность светового потока, входящего через раствор, через I0 . разделим длину, занимаемую раствором в кювете, на b участков. Когда свет пройдёт через первый участок поглощающего свет раствора, интенсивность света ослабится в n раз и в конце первого участка будет равна
где n – число больше единицы. Конец первого участка является в то же время началом второго. Во второй участок раствора попадает, таким образом, поток света с интенсивностью I1 . при прохождении света через второй участок снова произойдёт ослабление света в такой же степени, т.е. в n раз. Таким образом, в конце второго участка интенсивность светового потока равна:
Принимая во внимание уравнение (4), получим:
Таким образом, когда поток света пройдёт через всю толщину (т.е. согласно условию через b участков), интенсивность выходящего потока равна
Отсюда
или, логарифмируя и вводя полученное значение в уравнение (3), находим выражение, связывающее оптическую плотность D с толщиной слоя:
где lgn – постоянная величина, характерная для данного вещества. Как видно из уравнения (9), численное значение lg n можно найти, установив оптическую плотность раствора в кювете длиной 1 см (b=1). Зависимость между оптической плотностью и толщиной слоя, выражаемая уравнением (9), называется законом Бугера – Ламберта. Зависимость (8) можно также вывести из величины поглощения в бесконечно малом слое, интегрированием на всю толщину кюветы. Для этого, аналогично сказанному выше, рассмотрим поглощение монохроматического света телом с параллельными стенками. Бесконечно тонкий слой поглощает долю энергии входящего в него параллельного монохроматического пучка света, пропорциональную толщине слоя db. Тогда относительное уменьшение интенсивности светового потока
где k – коэффициент, характеризующий поглощение света данным телом и зависящий от свойств данного тела. Этот коэффициент в широких пределах не зависит от интенсивности светового потока, только при очень больших её значениях k перестаёт быть постоянным и наблюдается зависимость k от I, т.е. возникает нелинейность поглощения и k перестаёт быть пропорциональным I. Проинтегрировав уравнение (10), получим:
Логарифмируя уравнение (10), получим:
Постоянный коэффициент k аналогичен величине lg n из уравнения (9), т.е. k=lg n. Из рассматриваемого закона вытекает: отношение интенсивности светового потока, прошедшего через слой раствора, к интенсивности падающего светового потока не зависит от абсолютной интенсивности падающего светового потока; если толщина слоя раствора увеличивается в арифметической прогрессии, интенсивность светового потока, прошедшего через него, уменьшается в геометрической прогрессии.
Закон Бэра
Ослабление интенсивности светового потока при прохождении через раствор зависит от количества поглощающих свет центров на пути светового потока. Рассмотрим поглощение света раствором окрашенного соединения при условии, что состав и структура этого соединения не меняется с изменением его концентрации. Примером такого раствора может быть хромат калия; для постоянства pH при разбавлении к раствору прибавляют тетраборат натрия. Если налить немного этого раствора в высокий цилиндр и измерять поглощение света сверху, т.е. в полном слое. Согласно условию, общее количество поглощающих свет центров остаётся постоянным при разбавлении раствора, поэтому общее светопоглощение также не изменяется. При разбавлении раствора в n раз концентрация раствора уменьшится в n раз, а толщина слоя в цилиндре во столько же раз соответственно увеличится, поэтому общая оптическая плотность не изменится. Следовательно:
где k – коэффициент пропорциональности, обозначаемый обычно через Пусть раствор, концентрация которого С1 , при толщине слоя b1 имеет такую же оптическую плотность, как и раствор того же вещества при большей толщине слоя b2 . Очевидно, во втором растворе концентрация С2 вещества меньше, чем в первом растворе в отношении:
С1: С2 = b2 : b1 (14) С1 b1 = С2 b2 (15)
Эту зависимость установил в 1852 г Бэр и экспериментально проверил её измерениями оптической плотности газообразного хлора при различных давлениях. Объединяя уравнения (9) и (14), можно написать:
Эта зависимость называется законом Бугера – Ламберта – Бэра и применяется при различных расчётах в фотометрическом анализе. Если концентрация С выражена в молях на литр, а толщина слоя b – в сантиметрах, то коэффициент Также нужно сказать, что источниками ошибок при фотометрии могут быть отклонения от закона Бугера – Ламберта – Бэра и особенности возникающей окраски. Отклонения от закона Бугера – Ламберта – Бэра могут быть вызваны и посторонними веществами, присутствующими в растворе.
|



 (3)
(3) (4)
(4) (5)
(5) (6)
(6) (7)
(7) (8)
(8) (9)
(9) пропорционально толщине слоя db, через который прошёл световой поток:
пропорционально толщине слоя db, через который прошёл световой поток: (10)
(10) (11)
(11) (12)
(12) (13)
(13)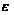 .
. (16)
(16)