 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| КЛЕТОЧНАЯ ТЕОРИЯ ГЕМОСТАЗА 12
Сосудистая стенка Сосудистый эндотелий Нормальный эндотелий действует как мощная антикоагулянтная поверхность, предотвращая тромбообразование. Это достигается благодаря: 1. Выделение в кровоток физиологических антигоагулянтов (глюкозаминогликаны, комплексы гепаран-антитромбин III, ингибитор пути тканевого фактора (TFPI) протеин С и S). 2. Активация фибринолиза – образование плазминогена, тканевого активатора плазминогена (t-PA), урокиназы (u-PA), тромбомодулина, протеина С. Тромбомодулин Антикоагулянтная активность эндотелия связана с наличием специфического мембранного белка - тромбомодулина. На поверхности интактного эндотелия содержится значительное количество ТМ. Тромбомодулин с высокой аффинностью связывает тромбин, меняя «направленность» его действия. Комплекс тромбин-тромбомодулин активирует протеин С. Последний в комплексе с протеином S ингибирует активные факторы каскада коагуляции Va и Villa. Другой функцией комплекса тромбин-тромбомодулин является активация прокарбоксипептидазы Y до активного ингибитора - карбоксипептидазы Y или тромбин-активируемого ингибитора фибринолиза (TAFI), который замедляет фибринолиз.
3. Ингибирование адгезии и агрегации тромбоцитов, вазодилатация (продукция простациклина, оксида азота, АДФазы). ПРОСТАЦИКЛИН – простагландин I, мощный сосудорасширяющий и антиагрегационный агент, антагонист тромбоксана A2. Антиагрегационное действие простациклина связано со способностью активировать аденилатциклазу тромбоцитов. Это ведет к увеличению синтеза цАМФ, удалению ионов Са2+ в пулы хранения и снижению способности тромбоцитов к агрегации
Эндотелий ингибирует активацию тромбоцитовза счет выработки простациклина
ОКСИД АЗОТА (NO) – эндотелиальный фактор релаксации. NO поддерживает нормальный базальный тонус сосудов, нормализуя их реактивность, способность к дилятации. Обладает антиагрегационным, антиадгезивным свойствами. ЭНДОТЕЛИАЛЬНЫЙ ФАКТОР ГИПЕРПОЛЯРИЗАЦИИ вызывает открытие калиевых каналов в гладких мышцах, что вызывает расслабление сосудов. В отличие от оксида азота этот фактор выделяется не постоянно, а только под действием некоторых стимулов: ацетилхолина, брадикинина, тромбина, гистамина, субстанции Р, АДФ, АТФ. НАТРИЙУРЕТИЧЕСКИЙ ПЕПТИД С-типа (НПС), ПНУФ (предсердный натрийуретический фактор - по другой терминологии) — один из трех членов семейства натрийуретических пептидов. В отличие от предсердного и мозгового натрийуретических пептидов этот фактор, по-видимому, образуется в основном в эндотелии и некоторых клетках крови и участвует в локальной регуляции сосудистого тонуса. НПС – вазодилятатор и дезагрегант.
4. Извлечение из кровотока активированных факторов свертывания.
Кроме того эндотелий обеспечивает структурную и функциональную целостность сосудистой стенки, межклеточное взаимодействие и образование диффузного барьера, который предотвращает попадание крови из внутрисосудистого пространства во внесосудистое (синтез в субэндотелий коллагена, эластина фибронектина и других веществ).
Но после стимуляции или травмы эндотелий трансформируется в мощную прокоагулянтную поверхность. Повреждение стенок сосудов, что сопровождается оголением субэндотелия, способствует активации свертывания крови и первичного гемостаза следующими путями: 1. Выделение в кровь тканевого тромбопластина, фактора V и других прокоагулянтов 2. Продукция плазменных кофакторов адгезии и агрегации тромбоцитов ( ф. Виллебранда (VWF), фактора активации тромбоцитов (PAF) и др.) 3. Выделение вазоконстрикторов (эндотелин-1, норадреналин) 4. Продукция ингибиторов фибринолиза (PAI-1, PAI-2), на стимулированных эндотелиальных клетках снижается количество тромбомодулина. 5. Происходит изменение фосфолипидного состава наружной поверхности мембраны эндотелиальных клеток с появлением рецепторов для ферментных комплексов коагуляционного каскада.
Наиболее значимыми стимулами, активирующими эндотелиоциты, являются воспалительные цитокины, эндотоксины, тромбин, гистамин, гипоксия, свободные радикалы кислорода, турбулентные потоки крови, внутриклеточные инфекционные агенты, механические повреждения, иммунные комплексы и др. Тромбоциты Тромбоциты, или кровяные пластинки, вырабатываются мегакариоцитами костного мозга. Это безъядерные фрагменты их цитоплазмы. У здорового человека количество тромбоцитов в периферической крови подвержено значительным колебаниям в течение суток - от 150 до 350 • 109/л. Средняя продолжительность жизни тромбоцитов в норме в пределах 7 дней. В состоянии покоя тромбоцит представляет собой дискообразный осколок мегакариоцитов с гладкой цитоплазматической мембраной, поддерживаемой микротубулиновым кольцом. Важное свойство мембраны интактных тромбоцитов - это разный фосфолипидный состав наружной и внутренней поверхности. Основные фосфолипиды, входящие в состав тромбоцитов, можно разделить на 2 группы: 1) не обладающие прокоагулянтной активностью холиновые: фосфатидилхолин (ФХ) и сфингомиелин (СФ), 2) обладающие прокоагулянтными свойствами кислые: фосфатидилсерин (ФС), фосфатидилэтаноламин (ФЭ) и фосфатидилинозитол (ФИ). Фосфолипиды первой группы распределены как на наружней, так и на внутренней поверхности клеточной мембраны неактивированных тромбоцитов. Фосфолипиды второй группы в неактивированных тромбоцитах локализованы преимущественно на внутренней поверхности клеточной мембраны. В процессе активации тромбоцита концентрация ФС, ФЭ и ФИ на наружной поверхности значительно возрастает и образует прокоагулянтную поверхность, необходимую для фиксации, активации и взаимодействия плазменных белков гемостаза. Кроме того, это перераспределение меняет вязкость клеточной мембраны, что тоже важно для протекания гемостатических реакций. Кислые фосфолипиды мембраны тромбоцитов - ФС, ФИ и ФЭ называют фактором 3 тромбоцитов (ф.З, PF3), или тромбоцитарным тромбопластином.
Цитоплазматическая мембрана тромбоцитов внедряется внутрь клетки с образованием многочисленных переплетенных канальцев, связанных с внеклеточным пространством. Эта система называется «открытой канальцевой системой» (ОКС). Сократительные филаменты распространяются по всей цитоплазме и обуславливают изменение формы тромбоцита при его активации. В цитоплазме тромбоцита обнаруживается 4 типа гранул: а-гранулы – содержат факторы, участвующие в процессах гемокоагуляции, воспаления, иммунных реакций, репарации (антигепариновый фактор, β-тромбоглобулин (ингибитор синтеза простациклина эндотелиоцитами), PAI-1, vWF, акцелератор-глобулин (аналог фактора V плазмы), фXI, фXIII, ВМК, тромбоцитарный фактор роста (PDGF) –стимулятор пролиферации эндотелиоцитов, гладкой мускулатуры и фибробластов, фибронектин (укрепляет тромб на повреждённой поверхности). Плотные гранулы – представляют собой хранилище АДФ, АТФ, серотонина и ионов кальция. Лизосомальные гранулы – содержат гидролитические ферменты. На мембране тромбоцитов экспрессируются большое количество рецепторов, но наибольший интерес представляют гликопротеиновые рецепторы адгезии и агрегации (GP). Гликопротеин I состоит из двух дисульфидносвязанных субъединиц - Iа и Ib. GP Iа является рецептором адгезии к коллагену а и необходим для полноценной адгезии (прилипания) тромбоцита к субэндотелию. Гликопротеин GP1b является рецептором для фактора Виллебранда и для тромбина. Взаимодействие GPIb с фактором Виллебранда (или тромбином) приводит к активации тромбоцитов. При аномалии тромбоцитов содержание гликопротеина Ib в тромбоцитах резко снижено и пластинки не агрегируют под действием тромбина (болезнь Бернара-Сулье). GP IIb/IIIa – рецептор агрегации взаимодействующий с фибриногеном. Особенность – роль рецептора IIbIIIa осуществляет только на активированных тромбоцитах (активация тромбоцитов приводит к конформационным изменения GPIIbIIIa и связыванию с фибриногеном). При врожденном дефиците GPIIbIIIa развивается тромбоастения Гланцмана, при которой тромбоциты не способны связываться с фибриногеном. Тромбоастения Гланцмана характеризуется тяжелыми рецидивирующими кровотечениями слизистых.
Рецепторы адгезии покоящихся тромбоцитов обладают высоким сродством к своим лигандам, что обеспечивает спонтанную адгезию тромбоцитов. GP IIb-IIIa (рецептор агрегации) – замаскирован, поэтому тромбоциты в состоянии покоя не способны к агрегации. Однако, активация тромбоцитов приводит к конформационному изменению GP IIb-IIIa, которое способствует связыванию фибриногена с тромбоцитарной мембраной, что в свою очередь приводит к агрегации. Функции тромбоцитов: 1. Ангиотрофическая – способность поддерживать нормальную структуру и функцию сосудов 2. Способность поддерживать спазм поврежденных сосудов путем секреции вазоактивных веществ (норадреналин, серотонин, тромбоксан и т.д.) 3. Способность закупоривать поврежденные сосуды путем образования тромбоцитами белого тромба. Это зависит от: А) адгезии – приклеивании тромбоцитов к субэндотелию Б) агрегации – склеивание тромбоцитов друг с другом В) образование, накопление и секреция факторов адгезии и агрегации Г) участие в плазмокоагуляции. Одним из важнейших клеточных эффектов в системе гемостаза является реакционная способность тромбоцитов к образованию агрегатов и адгезии к чужеродным поверхностям. При контакте с коллагеном субэндотелия поврежденного сосуда тромбоциты адгезируют к нему через белковые мостики - VWF, образуя однослойную выстилку, к которой из истекающей крови налипают другие тромбоциты. Этот эффект носит название агрегация.
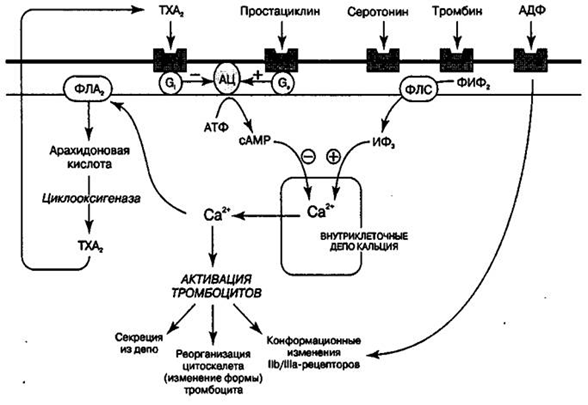
Сосудисто-тромбоцитарный (первичный) гемостаз обеспечивается сосудистой стенкой и тромбоцитами. Цель – начальная остановка кровотечения Результат – образование тромбоцитарной пробки (белого тромба) в месте повреждения сосуда. Этапы: 1. Местная вазоконстрикция. Незамедлительной реакцией на травму сосудистого эндотелия является вазоконстрикция. Эта преходящая реакция длительностью менее 60 с приводит к снижению кровотока, что улучшает взаимодействие между тромбоцитами, факторами свертывания крови и поврежденным участком. Первичный сосудистый спазм быстро сменяется парезом прекапиллярных сфинктеров и повышением проницаемости капилляров. Это связано вначале с действием гистамина, высвобождающегося из тучных клеток соединительной ткани в очаге поражения, а затем – с включением калликреин-кининовой системы. Ведущую роль в модуляции этих изменений выполняет эндотелин. Эндотелин (ЕТ) - пептидный гормон, состоящи 21 аминокислоты, относится к группе цитокинов, имеет 3 изоформы (ЕТ-1, ЕТ-2 и ЕТ-3). Образуется эндотелин из предшественника пре-про-ЕТ при участии металлопептидазы - эндотелинпревращающего фермента. ЕТ-1 - наиболее сильный вазоконстриктор из всех известных факторов, доминирует в эндотелиальных клетках сосудов человека. Он также присутствует в небольших количествах в гладких мышечных клетках (ГМК) и кардиомиоцитах. ЕТ не хранится в клетках, а постоянно синтезируется de novo. Синтез ЕТ и освобождение его из эндотелиальных клеток стимулируют тромбин, адреналин, ангиотензин, вазопрессин, некоторые цитокины. Большая часть ЕТ секретируется внутрь сосудистой стенки, где расположены специфичные высокоаффинные рецепторы. ЕТ, секретируемый наружу, взаимодействует с собственными рецепторами на клеточной мембране, а также стимулирует ангиотензинпревращающий фермент (АПФ), который переводит неактивный ангиотензин I в вазоконстриктор ангиотензин II. Рецепторы для эндотелина сопряжены с G-белками, присутствуют в 2 формах: ЕТ-А и ЕТ-В. Рецепторы ЕТ-А характеризуются высокой аффинностью и постоянно экспрессированы в миокарде на ГМК сосудов. Они обеспечивают прямое вазоконстрикторное действие эндотелина за счет активации поступления Са2+ в клетку через неселективные ионные каналы. Рецепторы ЕТ-В экспрессированы на эндотелиальных клетках и ГМК в отдельных сосудистых бассейнах. Стимуляция ЕТ-В сопровождается освобождением N0 (вазодилататор), тромбоксана (вазоконстриктор) и PGI2 (вазодилататор). Таким образом, один и тот же фактор реализует две противоположные сосудистые реакции (сокращение и расслабление), вызываемые различными химическими механизмами. Адгезия тромбоцитов А) непосредственное прилипание тромбоцитов к коллагену посредством рецепторов GP В) прилипание тромбоцитов к коллагену и фибронектину при помощи фактора Виллебранда (белок сыворотки крови имеющий центры связывания с тромбоцитами, коллагеном и фибронектином). Фактор Виллебранда (vWF) - один из самых больших гликопротеидов плазмы, имеет молекулярную массу от 540 до нескольких тысяч кДа, содержит в цепочке более 2000 аминокислот. актор Виллебранда состоит из ряда полимеров прогрессивно увеличивающейся молекулярной массы: разделяют легкие, средние, тяжелые и сверхтяжелые мультимеры. Молекулярная масса vWF варьирует от 540 кДа у димеров до 20 тысяч кДа у самых крупных мультимеров, содержащих от 50 до 100 субъединиц. Самым большим тромбогенным потенциалом обладают молекулы vWF с наибольшей молекулярной массой. В плазме нет мономеров фактора Виллебранда, он всегда образует комплексы. Концентрация vWF в плазме составляет примерно 10 мкг/мл. Основными функциями фактора Виллебранда являются: • опосредование адгезии тромбоцитов к субэндотелиальным структурам, в первую очередь • связывание свободного фактора VIII и защита его молекулы от преждевременной инактивации (участие во вторичном плазменном гемостазе). Молекулы vWF специфически связываются с рецепторами тромбоцитов GPIb и коллагеном субэндотелия. Это обеспечивает прочную фиксацию тромбоцитов к субэндотелиальным структурам. Помимо GPIb, с фактором Виллебранда также связывается GPIIb-IIIа. Возможно, что это взаимодействие является ключевым в процессе агрегации в местах сосудистого русла с высокой скоростью тока крови. При взаимодействии рецепторов тромбоцитов с лигандами происходит активация Са2+–инозитолфосфатного механизма передачи сигнала через мембрану. В результате активируется фермент фосфолипаза А2, которая высвобождает арахидоновую кислоту из мембранных фосфолипидов. Арахидоновая кислота окисляется по циклооксигеназному пути с образованием тромбоксана А2, который секретируется в реакции «высвобождения». С другой стороны, ионы кальция активируют фосфорилирование легких цепей миозина и сокращение тромбостенинового кольца, в результате чего гранулы по микротрубочкам секретируются и высвобождаются факторы активирующие адгезию и агрегацию.
При сокращении тромбостенина возникает контракция тромбоцитов, происходит изменение физико-химических свойств мембраны тромбоцита вследствие транслокации аминосодержащих фосфолипидов (фосфатидилаэтаноламинов, фосфатидилсеринов). Мембрана приобретает свойство образовывать псевдоподии, в результате резко увеличивается поверхность. Контрактированные тромбоциты приобретают способность склеиваться друг с другом в результате изменения конформации рецептора GP IIb-IIIa. 3. Агрегация тромбоцитов. После фиксации тромбоцитов на субэндотелии, они распластываются на сосудистой стенке. Другие тромбоциты покидают кровоток и оседают на распластанных тромбоцитах. В конечном итоге формируется гемостатическая пробка – группа активированных тромбоцитов, соединенных друг с другом нитями фибриногена и прикрепленных фактором Виллебранда к субэндотелию. Кроме того, поверхность тромбоцитов изменяется, т.е. появляется новая, «чужеродная» поверхность, т.е. формируетсятромбоцитарный тромбопластинна котором происходит фиксация и активация факторов свертывания крови.
КОГУЛЯЦИОННЫЙ ГЕМОСТАЗ Образовавшаяся в результате первичного гемостаза тромбоцитарная пробка достаточно рыхлая. Этого достаточно для окончательной остановки капиллярного кровотечения. Однако в более крупных сосудах она постепенно вымывается током крови, что может привести к возобновлению кровотечения. Поэтому первичная тромбоцитарная пробка («белый» тромб) укрепляется фибрином с включением других форменных элементов крови, в результате чего образуется «красный» тромб. Это происходит в результате активации коагуляционного (вторичного) гемостаза. Вторичный, или коагуляционный, гемостаз – многоэтапный ферментативный процесс, в котором участвуют ферментативные белки плазмы и тканей, надмолекулярные образования и ионы кальция, при котором происходит формирование фибринового сгустка, который повышает плотность тромба и закрепляет его на сосудистой стенке в месте повреждения. Цель –окончательная остановка кровотечения. Результат –образование фибрина и формирование красного тромба.
Неферментативные факторы свертывания крови (V и VIII) Факторы Va и VIIIa не обладают протеолитической активностью, а являются кофакторами для реакций активации фактора X (кофактор IXa фактрора – VIIIa, входит в состав теназного комплекса) и реакции превращения протромбина (II) в тромбин (IIa) (кофактор Ха фактора – Va, входит в состав протромбиназы). VIII и V факторы активируются тромбином, методом частичного протеолиза. Ингибитором VIIIa и Va служит активированный протеин С (APC).
В коагуляционном гемостазе условно выделяют 3 стадии: I стадия – это активация фермента тромбиназы (Ф.Xа) II стадия – это активация под действием тромбиназы протромбина (Ф.II) и переход его в активный фермент – тромбин (Ф.IIa) III стадия – переход растворимого фибриногена (Ф. I) в нерастворимый фибрин (Ф.I ais) под действием тромбина.
Повреждение TF + VIIa (внешняя теназа)
Протромбин (Ф.II)
Тромбиназа фибриноген (Ф.I) Ф.Xа
Поверхностью для активации проконвертина (VII) является тканевой тромбопластин – тканевой фактор (TF) (Ф.III). Этот комплекс (Ф.III, Ф.VIIа, ионы кальция) на поверхности контрактированных тромбоцитов (ф.3) активирует тромбиназу (Х). Тромбиназа связывается при участии Ф.V и ионов кальция с поверхностью тромбоцитарных фосфолипидов (ф.3) и активирует тромбин. Тромбин осуществляет последовательное превращение фибриногена в нерастворимый фибрин. Полимеризация фибриногена проходит в несколько этапов: 1. под действием тромбина происходит отщепление фибринопептидов А, фибриноген превращается в дезАА-фибриноген 2. сборка дезАА-фибриногена в протофибриллы в шахматном порядке 3. отщепление фибринопептидов В 4. ускорение сборки протофибрилл, образование фибриновых волокон 5. ветвление волокон с образованием трехмерной фибриновой сетки. 6. образование под действием XIIIa изопептидных связей между цепями, что приводит к повышению механической стабильности фибрина и его устойчивости к лизису.
Образуется трехмерная сетчатая структура, стабилизирующая первичную пробку, в которой задерживаются форменные элементы крови.
КЛЕТОЧНАЯ ТЕОРИЯ ГЕМОСТАЗА
В процессе образования свертывания выделяют несколько стадий. · Инициации · Амплификации · Распространения · Терминация
В стадию инициации на тканевом тромбопластине генерируются начальные порции промбина, необходимые для активации агрегации и секреции тромбоцитов. В эту стадию свертывание определяется производством Xa фактора внешней теназой. Однако фактор Xa быстро ингибируется и не может обеспечить достаточные количества тромбина по мере роста тромба (фаза распространения). Поэтому возникает “петля амплификации”, которая заключается в активации внутренней теназы (IXa, VIIIa). В фазе распространения сгустка фактор Xa образуется внутренней теназой. Однако лимитирующий компонент внутренней теназы, фактор IXa, производится внешней теназой. При дальнейшем росте сгустка дополнительный фактор IXa производится фактором XIa в петле положительной обратной связи – «тромбиновый взрыв».
12 |












 Тромбин (Ф.IIa)
Тромбин (Ф.IIa) Фибрин (Ф.Iais)
Фибрин (Ф.Iais)
 Активация факторов свертывания происходит на «чужеродных» поверхностях – тромбопластинах. Тромбопластином для тромбина и тромбиназы являются фосфолипиды агрегированных тромбоцитов – тромбоцитарный тромбопластин (ф.3).
Активация факторов свертывания происходит на «чужеродных» поверхностях – тромбопластинах. Тромбопластином для тромбина и тромбиназы являются фосфолипиды агрегированных тромбоцитов – тромбоцитарный тромбопластин (ф.3).

