ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Лямблия (изображение получено в сканирующем электронном микроскопе)
Лямблии в мазке (микрофотография)
Лямблия (изображение получено в сканирующем электронном микроскопе)
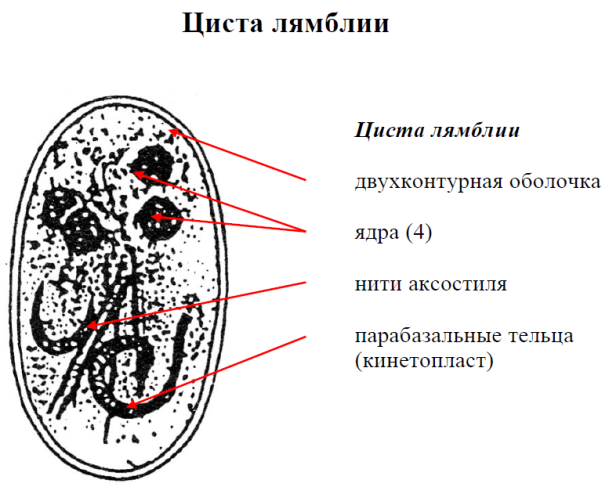
Распространенность лямблиоза повсеместная и зависит от особенностей диеты, водоснабжения и уровня санитарно-гигиенических навыков населения. Среди детей инфицированность существенно выше и в организованных детских коллективах доходит до 40 %; среди взрослого населения в развитых странах инфицированность составляет 3–5 %, а в развивающихся — 10–15 %. Лямблиоз весьма значим в оценке здоровья населения по рекомендациям ВОЗ. Морфологические особенности. Лямблии существуют в двух формах: вегетативной (трофозоит) и цистной.
Вегетативная форма (трофозоит) имеет грушевидную симметричную форму тела размером 9 - 12 мкм. Передний конец тела широкий, закругленный, задний (хвостовой) — заостренный. На вентральной поверхности тела имеется присасывательный диск. Лямблия имеет 2 ядра и 4 пары жгутиков, которые являются органеллами движения. По средней линии тела лямблии проходят две опорные нити — аксостили, которые делят клетку на две симметричные половины. С помощью вентрального присасывательного диска лямблии прикрепляются к микроворсинкам тонкого кишечника. Питаются они только переваренной пищей хозяина путем пиноцитоза. Органоиды пищеварения и осморегуляции отсутствуют. Лямблии — анаэробы. Они лишены митохондрий и аппарата Гольджи. Цисты овальные (размер 8–14 - 7–11 мкм, в среднем 12 - 8 мкм). В их цитоплазме содержится 2 или 4 ядра и свернутый жгутиковый аппарат.
Жизненный цикл. Вегетативные формы (трофозоиты) размножаются путем продольного деления. Во внешнюю среду с фекалиями хозяина попадают как трофозоиты, так и образующиеся в кишечнике цисты. Выживают во внешней среде только цисты, которые попадают в организм человека перорально (с зараженной водой или пищей). Инвазионная стадия — циста. Пути заражения человека. Источником инвазии служит больной человек или цистоноситель. Передача лямблиоза осуществляется пероральным путем. Цисты лямблий выделяются с фекалиями больного и могут длительно сохраняться во внешней среде, а в воде — до 70 суток. Цисты лямблий устойчивы к хлору. Они хорошо сохраняются в пыли, на плохо промытых овощах, ягодах, зелени. Возможно распространение при помощи механического переносчика (комнатные мухи). Локализация в организме человека. Двенадцатиперстная кишка и тонкий кишечник. Действие на организм человека. Лямблии механически раздражают и блокируют слизистую оболочку двенадцатиперстной кишки и тонкого кишечника, вследствие чего пища не переваривается, а гниет — начинается усиленное размножение гнилостных бактерий и дрожжевых клеток. В просвете кишечника накапливаются продукты жизнедеятельности и распада простейших, что приводит к интоксикации организма. Нарушается работа кишечника, возникают патологические изменения в желудке, тонком и толстом кишечнике, желчном пузыре, желчевыводящих путях, поджелудочной железе, печени. В желудочно-кишечном тракте нарушается всасывание белков, жиров, углеводов и витаминов, что приводит к истощению организма. Диагностика. Микроскопические исследования дуоденального содержимого на выявление трофозоитов, исследования фекалий больного на наличие цист лямблий, проведение иммуноферментного анализа на антитела к лямблиям в крови. Каждый из этих методов не дает 100%-й информации, они взаимно дополняют друг друга и оцениваются в комплексе. Профилактические мероприятия. Выявление и лечение больных, кипячение воды, уничтожение мух, защита водоемов и почв от загрязнения фекалиями, соблюдение правил личной гигиены, санитарно-просветительская работа среди населения.
Отряд Trichomonadida Трихомонады(Trichomonas) — жгутиковые простейшие из семейства Trichomonadidae класса Zoomastigophora. Клетки трихомонад грушевидной формы, длиной 5–30 мкм. На переднем конце клетки имеют 3–5 свободных жгутиков, один жгутик проходит вдоль тела и соединяется с его поверхностью ундулирующей мембраной. По оси тела проходит аксостиль, который слегка выступает у заднего заостренного конца тела. В передней части тела имеется небольшой цитостом (клеточный рот). Рядом с ним, позади группы парабазальных тел, расположено ядро. Ядро одно. Трихомонады питаются бактериями, которых заглатывают с помощью цитостома. Размножаются трихомонады продольным делением. Цист не образуют. В организме человека могут паразитировать 3 вида трихомонад: ♣ Trichomonas vaginalis (влагалищная трихомонада) паразитирует в мочепо- ловом тракте; ♣ Trichomonas hominis (кишечная трихомонада) паразитирует в толстом кишечнике; ♣ Trichomonas tenax (ротовая трихомонада) паразитирует в полости рта.
Кишечная трихомонада(Trichomonas hominis (intestinalis)) — возбудитель кишечного трихомониаза, антропоноза. Паразит длиной 5–15 мкм имеет 4 (иногда 3–5) свободных жгутиков. Форма тела может значительно изменяться. Кишечная трихомонада (Trichomonas hominis)
Цитоплазма имеет зернистую структуру и содержит пищеварительные вакуоли. Питание паразита происходит путем поглощения бактерий и других частиц. Ядро крупное, овальной формы. Паразит существует только в вегетативной форме (трофозоит), цист не образует. Локализация в организме человека. Т. hominis локализуется в толстой и слепой кишках, иногда — в нижних отделах тонкого кишечника. Заражение происходит через фекалии, в которых при отсутствии высыхания трихомонады могут оставаться жизнеспособными много часов и даже несколько суток. Мухи, поедая фекалии, содержащие вегетативные формы трихомонад, могут выделять со своими испражнениями подвижные трихомонады и заражать ими пищу. Патогенная роль Т. hominis недостаточно точно установлена, хотя описано внедрение его в полость желез кишечной стенки и в подлежащие ткани. Кишечная трихомонада вызывает проблемы, которые связаны с деятельностью кишечника, среди которых колит, энтероколит, холецистит. Кроме того, деятельность трофозоитов кишечной трихомонады может вызывать диарею, нарушение функций кишечника. Лабораторная диагностика. Трофозоиты Т. hominis обнаруживаются в жидких фекалиях больного. Профилактические мероприятия. Личная профилактика, улучшение санитарно-гигиенических условий, выявление и лечение больных, борьба с мухами, санитарно-просветительская работа среди населения. Влагалищная трихомонада(Trichomonas vaginalis) — возбудитель мочеполового трихомониаза, антропоноза. Паразит распространен повсеместно.
Локализуется во влагалище, цервикальном канале и уретре у женщин, у мужчин — в уретре и простате. Клетка достигает несколько больших размеров, чем клетка Т. hominis (до 30 мкм), и имеет все характерные морфологические признаки клеток трихомонад. Влагалищная трихомонада существует только в вегетативной форме и цист не образует.
Пути заражения человека. Инфекция передается от человека к человеку при половом контакте (контаминативное заражение). Действие на организм человека. При заражении трихомонадами возможно развитие острого или хронического заболевания, а также бессимптомного носительства у мужчин. Заболевание проявляется в воспалении слизистой облочки пораженных органов мочеполовой системы. Т. vaginalis может служить причиной кольпита (воспаление слизистой оболочки влагалища). Диагностика. У женщин исследуют выделения из влагалища, у мужчин — выделения из мочеиспускательного канала и секрет простаты. Результат общего мазка подтверждают более точными методами исследования — ПЦР или посевом. Профилактические мероприятия. Личная гигиена, санитарно-просветительская работа, выявление и лечение больных. Ротовая трихомонада(Trichomonas tenax) до сих пор относительно мало изучена, несмотря на то что она очень распространена.
Морфологические особенности. Клетка Trichomonas tenax неотличима от клетки Т. hominis. Локализация в организме человека. Ротовая полость, дыхательные пути, миндалины, десны. Действие на организм человека. К следствиям жизнедеятельности ротовой трихомонады иногда относят кариес и пародонтоз. Полагают, что чрезмерное размножение ротовой трихомонады может привести к ЛОР-заболеваниям.
Отряд Kinetoplastida Трипаносомы(Trypanosoma) — род паразитических одноклеточных простей ших, которые паразитируют на позвоночных хозяевах и вызывают заболевания, среди которых наиболее известны африканский трипаносомоз («сонная болезнь») и американский трипаносомоз (болезнь Чагаса). Резервуаром для трипаносом в основном служат млекопитающие, а специфическим переносчиком — насекомые. Морфологические особенности. Тело трипаносом продолговатое, узкое, имеет жгутик и ундулирующую мембрану.
Митохондриальная ДНК трипаносом, называемая кинетопластной ДНК, состоит из комплекса больших и малых колец. Трипаносомы размножаются исключительно бесполым путем — продольным делением клетки. В жизенном цикле трипаносом различают несколько морфологических стадий, которые различаются по положению кинетопласта и жгутика:
¨ трипомастиготная форма (трипаносомная стадия) циркулирует в крови человека и животных. Тело паразита удлиненное, жгутик начинается в задней части тела, ундулирующая мембрана тянется через все тело; ¨ эпимастиготная форма (критидиальная стадия). В форме эпимастигот трипаносомы существуют в кишечнике насекомых-переносчиков. Клетки вытянутые, жгутик начинается в передней части тела близко от ядра, ундулирующая мембрана слабо выражена; ¨ промастиготная форма (лептомонадная стадия) — клетки продолговатой формы, кинетопласт и кинетосома находятся в передней части клетки, ундулирующая мембрана отсутствует; в этой стадии Т. cruzi существуют в кишечнике насекомых-переносчиков; ¨ амастиготная (лейшманиальная стадия) в организме человека образует Т. cruzi. Клетки овальные или круглые, небольших размеров, имеется ядро и кинетопласт, жгутик отсутствует; ¨ метациклическая форма (инвазионная стадия). Для этой формы характерно отсутствие свободного жгутика на конце клетки, кинетопласт и кинетосома находятся сзади ядра, имеется длинная ундулирующая мембрана. Род трипаносом интересен наличием механизма защиты от иммунной системы хозяина. Когда трипаносомы проникают в организм и обнаруживаются иммунной системой хозяина, у трипаносом активируются гены, ответственные за синтез поверхностных гликопротеинов (антигенов паразитов). В результате существующие мембранные гликопротеины заменяются другими, поэтому иммунная система хозяина не может распознать паразитов, что дает им время для размножения. Установлено, что геном трипаносом кодирует вероятность появления 22 вариантов специфических поверхностных антигенов у каждого штамма. Африканские трипаносомозы.Различают два типа заболеваний: острый родезийский трипаносомоз (восточноафриканская «сонная болезнь», возбуди- тель — Trypanosoma brucei rhodesiense) и хронический гамбийский трипаносомоз (западноафриканская «сонная болезнь», возбудитель — Trypanosoma brucei gambiense). Возбудители морфологически и серологически идентичны. Видовая идентификация возможна лишь по биологическим (заражение насекомых-переносчиков) и биохимическим признакам. Жизненный цикл. Передачу возбудителя осуществляют мухи р. Glossina (цеце). Природный резервуар составляют травоядные животные. При кровососании трипомастиготы проникают в организм мух цеце, превращаются в эпимастиготы и размножаются в кишечнике и слюнных железах. Через несколько недель в организме насекомого скапливаются инвазионные метациклические трипомастиготы, которые попадают в организм человека при укусе мухи цеце. Гамбийский трипаносомоз переносят мухи цеце Glossina palpalis и G. tachinoides, обитающие в зарослях по берегам рек и озер. Резервуарами возбудителя служат больной человек и домашние животные (крупный и мелкий рогатый скот). Хроническое течение болезни обусловливает длительное пребывание больного среди здоровых лиц, что повышает риск переноса возбудителя мухами (рис. 17). Родезийский трипаносомоз переносят мухи цеце G. morsitans, G. pallipides и G. swynnertoni, обитающие в саваннах Восточной Африки. Основной природный резервуар — различные мелкие антилопы (газели Томпсона, дукеры и бушбоки).
Наиболее часто заражение человека происходит при выпасе скота или охоте.
Действие на организм человека. Инкубационный период продолжается 2–3 недели. Через 2–3 дня на месте укуса мухи цеце образуется язва (трипаносомидный шанкр), но возможно и отсутствие внешних поражений. Клинические проявления на этом этапе отсутствуют, но паразиты бурно размножаются и поступают по лимфатической системе в кровоток. У некоторых пациентов можно наблюдать увеличение шейных и затылочных лимфатических узлов, где можно обнаружить скопления трипаносом (признак Уинтерботтома). Циркуляция возбудителя в крови достигает своего пика через 2–3 недели и вызывает развитие характерных симптомов. Пациенты испытывают приступы лихорадки с постоянно учащенным пульсом, болезненной лимфаденопатией, кожной сыпью и головной болью. Возможны психические расстройства. Цикличность проявлений вызвана заменой антигенов паразитов, вызвавших предшествующий приступ, новыми поверхностными антигенами. Поражения ЦНС. Поражения, вызванные гамбийской трипаносомой, развиваются медленно, поражение ЦНС наблюдают через несколько лет после начала заболевания. Родезийская трипаносома вызывает прогрессирующую болезнь с поражениями мозга, которые развиваются через 3–6 недель после начала заболевания. Развиваются сонливость, тремор конечностей, паралич, речь становится невнятной. Характерны кома, судороги, острая сердечная недостаточность и сильное истощение, которое приводит к смерти больного в течение 6–9 месяцев. Лабораторная диагностика. В начальной стадии заболевания возбудителя можно обнаружить в месте укуса, в крови (родезийский тип) или шейных лимфатических узлах (гамбийский тип). Готовят препараты методом толстой капли и мазки крови, окрашенные по Райту или Романовскому—Гимзе (цитоплазма голубая, ядро красное).
Следует помнить, что при симптомах поражения ЦНС кровь и лимфатические узлы трипаносом не содержат. В этом случае проводят поясничную пункцию спинного мозга для выявления трипаносом в спинномозговой жидкости. При отрицательном результате микроскопии проводят экспериментальное заражение лабораторных животных: исследуемый материал вводят белым мышам или крысам (подкожно или внутримышечно). На 2–3-е сутки в крови животных появляются паразиты. Серологические исследования выявляют антитела класса IgM в диагностических титрах у всех больных. Профилактические мероприятия. Выявление и лечение больных, выявление животных — резервуаров возбудителей, уничтожение мух цеце и мест их размножения (прибрежные заросли). Личная профилактика — защита от укусов мухи цеце.
Американский трипаносомоз(южноамериканский трипаносомоз, бо- лезнь Чагаса) — инфекция, вызываемая Trypanosoma cruzi; переносчики — клопы рода Triatoma (семейство Reduviidae): Т. dimidiala, Т. infestans и Т. megistus.
Заболевание достаточно широко распространено в Центральной и Южной Америке, где болезнью Чагаса болеют около 7 млн человек. Заболевание протекает остро у детей и носит хронический характер у взрослых; характерны лихорадка и осложнения со стороны сердечно-сосудистой системы и желудочно-кишечного тракта. Жизненный цикл. Основная особенность Trypanosoma cruzi: для размножения возбудитель обязательно должен проникнуть в клетки теплокровных животных и образовать амастиготы. Эпимастиготы развиваются в кишечнике клопа.
Природные резервуары болезни — крысы, кошки, собаки, свиньи, опоссумы, муравьеды, лисы, основной резервуар в дикой природе — броненосцы-армадиллы (dasypodidae). Пути заражения человека. Заболевание чаще регистрируют в сельской местности, где переносчики обитают в норах животных и хижинах крестьян. Клопы обычно кормятся ночью, кусая человека чаще в области глаз и губ (отсюда название «поцелуйные клопы»). При укусе клоп повреждает кожные покровы, что обеспечивает проникновение метациклических трипомастиготных форм в организм хозяина. Также возможны случаи трансплацентарного инфицирования плода и заражения с гемотрансфузиями. Действие на организм человека. Возбудитель способен инфицировать и разрушать практически все типы ядросодержащих клеток. В месте проникновения возникает опухоль кожи (чагома), чаще на лице, с увеличением регионарных лимфатических узлов. Через 1–3 недели после укуса наблюдают отеки век и увеличение околоушных лимфатических узлов. Острые симптомы обычны у детей до 1 года, в старших возрастных группах регистрируют хронические формы. Инфекция у новорожденных часто приводит к менингоэнцефалиту. Характерны поражения миокарда и головного мозга. В отсутствие лечения смертность достигает 90 %. Хроническая форма характерна только для взрослых, обычно болевших в детстве. Проявляется хроническим разрушением внутренних органов. Наиболее частая форма — сердечно-сосудистая патология (аритмии, экстрасистолии), выявляемая у 10 % населения эндемичных сельских районов. Реже встречается патология желудочно-кишечного тракта, обычно мегаколон (расширение части или всей ободочной кишки с гипертрофией ее стенки) и мегаэзофагус (увеличение нижней части пищевода). Иногда могут преобладать проявления со стороны эндокринной (микседема) и нервной (параличи) систем. Лабораторная диагностика. Острая форма диагностируется с помощью микроскопии мазков крови, пунктатов лимфатических узлов, селезенки и других органов. Поскольку в крови возбудитель присутствует в небольших количествах, то венозную кровь можно разводить цитратом и центрифугировать. Хроническая форма более трудна для диагностики. Проводят серологические исследования и ксенодиагностику, которая заключается в кормлении незараженных триатомовых клопов на больном человеке. Попавшие в кишечник насекомого трипаносомы активно размножаются, и через две недели в фекалиях зараженных клопов можно обнаружить паразитов. Также используют метод биопроб (заражение лабораторных животных кровью больного и исследование внутренних органов и крови животного через 3–4 недели на наличие у него трипаносом). Профилактические мероприятия. Уничтожение клопов с помощью инсектицидов, улучшение санитарно-бытовых условий населения. Выявление и лечение больных. Выявление домашних и диких животных — резервуаров возбудителя. Санитарно-просветительская работа среди населения. Лейшмании — возбудители лейшманиозов. Впервые подробное описание лейшманий (Leishmania tropica), вызывающих кожный лейшманиоз, дал П.Ф. Боровский в 1897 г. Виды рода Leishmania во многом морфологически идентичны, что затрудняет их классификацию. В настоящее время большинство современных учебных пособий использует классификацию Ламсдена (1974), выделяющую 4 группы возбудителей:
¨ группа L. tropica (L. tropica minor и L. tropica major) — возбудители кожных лейшманиозов Старого Света (Африка и Азия). К этой же группе можно отнести недавно выделенную L. aeрhiopica — эндемичный возбудитель кожного лейшманиоза в Эфиопии; ¨ группа L. mexicana (L. mexicana подвид mexicana, L. mexicana подвид amazoniensis, L. mexicana подвид pifanoi, а также L. mexicana подвид venezuelensis и, возможно, L. mexicana подвид garnhami) — возбудители кожных и диффузных кожных лейшманиозов Нового Света. К этой группе также относят L. peruviana и L. uta — эндемичных возбудителей кожных лейшманиозов в высокогорных районах Анд и Кордильер; ¨ группа L. braziliensis (L. braziliensis подвид braziliensis, L. braziliensis подвид guyanensis, L. braziliensis подвид panamensis) — возбудители кожно-слизистых лейшманиозов Нового Света; ¨ группа L. donovani (L. donovani подвид donovani, L. donovani подвид infantum, L. donovani подвид archibaldii) — возбудители висцеральных лейшманиозов Старого Света.
Морфологические особенности. Лейшмании проходят две стадии развития: амастиготную и промастиготную.
Жгутиковые формы (промастиготы) — подвижные, развиваются в организме насекомого-переносчика (москита). Клетка имеет веретеновидную форму, длиной 10–20 мкм. Кинетопласт расположен в передней части клетки; жгутик длиной 15–20 мкм. Размножаются промастиготные формы продольным делением. Безжгутиковые формы (амастиготы) паразитируют в клетках млекопитающих; клетки амастигот имеют овальную форму, длиной 2–6 мкм, содержат кариосому и ядро. Жизненный цикл. Лейшманиозы относят к группе трансмиссивных инфекций, переносчиками которых служат москиты родов Phlebotomus и Lutzomyia. Переносчики заражаются при кровососании на больных людях и животных. В кишечнике москита амастиготы превращаются в промастиготные формы, которые начинают делиться и через 6–8 суток скапливаются в глотке москита. При укусе человека или животного промастиготы проникают в ранку и внедряются в клетки кожи или внутренних органов — в зависимости от вида лейшманий. Определенная роль в распространении возбудителя лейшманиоза принадлежит фагоцитам. После проникновения в клетки млекопитающих промастиготы превращаются в амастиготы.
Лейшмания(Leishmania tropica) — возбудитель кожного лейшманиоза. Кожный лейшманиоз Старого Света (пендинская язва, алеппский, багдадский или восточный фурункул) — антропозооноз, природно-очаговое заболевание. Выделяют антропонозный, или городской (болезнь Боровского) лейшманиоз (возбудитель — L. tropica подвид major) и зоонозный, или пустынный (возбудители — L. tropica подвид tropica и L. aethiopica), лейшманиоз.
Природный резервуар возбудителя — мелкие грызуны (мыши, крысы, песчанки, суслики, даманы). Переносчики — москиты Phlebotomus papatasii. Кожный лейшманиоз распротранен в странах с сухим тропическим и субтропическим климатом. Жизненный цикл показан на рисунке. Действие на организм человека. Инкубационный период длится от 2 недель до 5 месяцев. По окончании инкубационного периода на коже образуется узел (папула). Отмечают увеличение регионарных лимфатических узлов. Папулы изъязвляются; дно язвы покрыто грануляционной тканью, края воспаленные, возможно формирование дочерних поражений. В зависимости от возбудителя наблюдают формирование «сухих» (L. tropica major) или «мокрых» (L. tropica tropica) безболезненных язв. Через 3–12 месяцев наблюдают спонтанное излечение с образованием грубого пигментированного шрама («печать дьявола»). Диагностика. Проводят микроскопию кусочков ткани, взятых со дна язвы, окрашенных по Романовскому—Гимзе. У больных обнаруживают амастиготы. Профилактические мероприятия. Борьба с москитами, уничтожение диких грызунов в районах, прилегающих к населенным пунктам. Защита от укусов москитов, профилактические прививки. Выявление и лечение больных людей. Санитарно-просветительская работа среди населения.
Лейшмания(Leishmania braziliensis) — возбудитель кожно-слизистых лейшманиозов. Кожно-слизистый лейшманиоз (лейшманиоз Нового Света, американский лейшманиоз, носоглоточный лейшманиоз, эспундия, болезнь Бреды) — группа заболеваний, вызываемых L. braziliensis подвид braziliensis, L. braziliensis подвид guyanensis, L. braziliensis подвид panamensis. В отдельную группу возбудителей выделяют L. peruviana и L. uta, вызывающих поражения кожи и слизистых оболочек в высокогорных районах Америки.
Жизненный цикл показан на рисунке. Эпидемиология. Заболевание распространено во влажных лесах Центральной и Южной Америки, природным резервуаром служат крупные лесные грызуны. Заболевания обычно регистрируют у рабочих, занятых на лесных и дорожных работах, и среди населения лесных поселков. Действие на организм человека. Первичные симптомы появляются через 1–4 недели после укуса переносчика и напоминают таковые при кожном лейшманиозе. Иногда клинические проявления заканчиваются на этом этапе. В большинстве случаев первичные поражения прогрессивно увеличиваются. Характерны безболезненные деформирующие поражения рта и носа (от 2 до 50 % случаев), которые распространяются на соседние участки с появлением язв на языке, слизистой оболочке щек и носовой полости. Возможно появление поражений через несколько лет после спонтанного исчезновения первичных очагов. Наблюдают разрушение носовой перегородки, твердого нёба и деструктивные поражения глотки. Заболевание сопровождают лихорадка, снижение массы тела и вторичные бактериальные инфекции. Диагностика. Микроскопия выделений из язв и биопсия поврежденных органов. Используют метод биопроб и внутрикожные пробы. Профилактические мероприятия. Борьба с москитами, защита от укусов москитов, выявление и лечение больных, санитарно-просветительская работа среди населения. Лейшмания(Leishmania donovani) — возбудитель висцеральных лейшманиозов. Выделяют висцеральный лейшманиоз (болезнь Лейшмена—Донована, кала-азар, лихорадка дум-дум), вызываемый L. donovani подвид donovani, восточноафриканский висцеральный лейшманиоз (возбудитель — L. donovani подвид archibaldii) и средиземноморско-среднеазиатский висцеральный лейшманиоз (детский лейшманиоз), вызываемый L. donovani подвид infantum. Клинические и эпидемиологические особенности существенно варьируют в зависимости от географии заболеваний.
Жизненный цикл показан на рисунке. Эпидемиология. Кала-азар регистрируют на всех континентах, исключая Австралию. Заболевания человека протекают остро и тяжело, с возможными смертельными исходами. Основные резервуары — грызуны, лисы, шакалы, дикобразы и собаки. В Восточной Индии и Бангладеш (где естественный резервуар — человек) эпидемии лейшманиоза регистрируют каждые 20 лет. Заболеванию наиболее подвержены дети. Локализация в организме человека. Клетки ретикуло-эндотелиальной системы (селезенка, печень, костный мозг, лимфатические узлы). Действие на организм человека. Промастиготы лейшманий циркулируют в кровотоке и поглощаются тканевыми макрофагами костного мозга, селезенки, печени и лимфатических узлов. В них паразиты размножаются, вызывая увеличение печени и селезенки с их последующей атрофией. Развивается анемия, истощение, интоксикация, кровоизлияния в кишечнике, диарея. У лиц со слабой пигментацией кожи можно наблюдать сероватые пятна на лице и голове (на фарси кала-азар — черная лихорадка). Без лечения заболевание часто приводит к смерти пациента. Диагностика. Обнаружение лейшманий в мазках из пунктатов селезенки, лимфатических узлов, костного мозга. Окончательный диагноз висцерального лейшманиоза ставят на основании обнаружения лейшмании при микроскопии мазков костного мозга, окрашенных по Романовскому. Для получения костного мозга проводят пункцию грудины.
Профилактические мероприятия всех видов лейшманиозов должны включать уничтожение переносчиков, обработку мест пребывания людей ядохимикатами и меры предохранения людей от укусов москитов (использование репеллентов, противомоскитных сеток и др.). Профилактика висцеральных лейшманиозов включает раннее выявление и лечение больных, регулярные осмотры домашних животных.
ТИП APICOMPLEXA. КЛАСС SPOROZOEA (СПОРОВИКИ) Все споровики являются паразитами животных и человека. Органеллы движения у них отсутствуют. Питание споровиков осуществляется за счет поглощения пищи всей поверхностью тела. Многие споровики — внутриклеточные паразиты.
Малярийный плазмодий(род Plasmodium) паразитирует у человека в эритроцитах и клетках печени, вызывая тяжелое трансмиссивное заболевание — малярию (антропоноз). У человека паразитирует четыре вида малярийных плазмодиев: ¨ Plasmodium vivax — возбудитель трехдневной малярии (tertiana) с приступами лихорадки через 48 часов; ¨ Plasmodium malaria — возбудитель четырехдневной малярии (quartana) с приступами через 72 часа; ¨ Plasmodium falciparum — возбудитель тропической малярии (tropica) с приступами через 24 или 48 часов; ¨ Plasmodium ovale — возбудитель малярии типа трехдневной (tertiana), встречается в Африке.
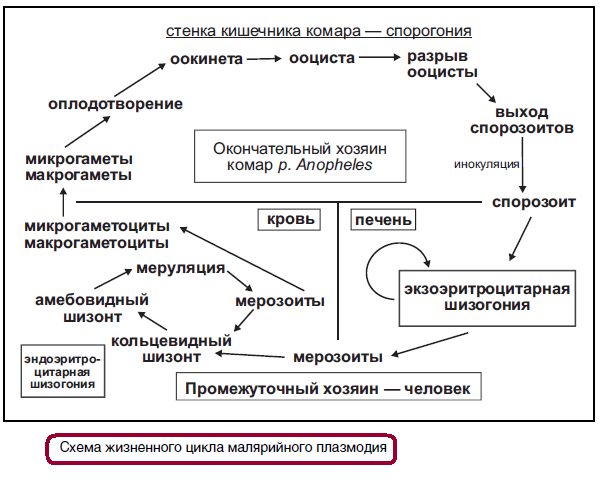
Жизненный цикл плазмодия происходит в двух стадиях (бесполой и половой) со сменой хозяев. Бесполое размножение происходит в организме человека (промежуточный хозяин), а половой процесс — в организме переносчика — самки комара рода Anopheles (основной хозяин). Морфология паразита зависит от стадии его развития.
Развитие малярийного плазмодия в организме человека. Человек заражается при укусе комара (инокулятивно), который вводит в кровь слюну со спорозоитами (инвазионная форма). Спорозоиты с током крови достигают клеток печени, где растут, приобретают амебоидную форму, размножаются множественным делением (шизогонией), проходя постепенно стадии трофозоита и шизонта. В процессе деления шизонта образуются молодые особи — тканевые мерозоиты (экзоэритроцитарный цикл). Тканевые мерозоиты выходят из поврежденной клетки печени и проникают в новые клетки, где снова проходят указанный цикл развития. Развитие малярийного плазмодия в ткани печени не вызывает ответной реакции организма.
Эндоэритроцитарные стадии развития малярийного плазмодия. Для дальнейшего своего развития тканевые мерозоиты должны проникнуть в эритроциты, в которых они растут, питаются цитоплазмой эритроцита, а также размножаются способом шизогонии. Отмечают следующие стадии развития паразита: 1) мерозоит — шаровидная форма. На препарате, окрашенном по Романовскому—Гимзе, видно голубую цитоплазму и ядро вишнево-красного цвета; 2) стадия кольца — в цитоплазме паразита появляется вакуоль, а сам он напоминает перстень; 3) амебоидный трофозоит — на этой стадии образуются псевдоподии и изменяется форма тела плазмодия. В цитоплазме трофозоита появляется пигмент меланин — продукт расщепления гемоглобина; 4) зрелый шизонт, который втягивает псевдоподии, закругляется и занимает почти весь эритроцит; 5) шизонт в стадии деления — происходит процесс шизогонии, в результате чего образуются эритроцитарные мерозоиты. Количество мерозоитов в делящемся шизонте зависит от вида плазмодия (от 6 до 24 мерозоитов). Процесс шизогонии сопровождается разрушением эритроцита и выходом в кровь мерозоитов и токсических продуктов обмена паразита, что и вызывает приступы лихорадки. Из плазмы крови мерозоиты снова проникают в эритроциты (однако большое количество их погибает), и процесс шизогонии повторяется. Каждая эритроцитарная шизогония (от мерозоита до мерозоита) у Pl. vivax и Pl. falciparum длится 48 часов, у Pl. malaria —72 часа, отсюда и приступы лихорадки через указанные промежутки. Кроме этого, в эритроцитах формируются незрелые половые формы паразита (гамонты) — макрогаметоциты и микрогаметоциты. Гамонты — это конечная стадия развития малярийного плазмодия в организме человека. Процесс созревания гаметоцитов происходит в кишечнике комара Anopheles, который получает их с кровью больного малярией. Развитие малярийного плазмодия в организме комара (Anopheles).В кишечнике комара плазмодий проходит половой цикл развития. Мужские и женские гаметоциты после созревания образуют гаметы, которые копулируют и образуют диплоидную зиготу, которая превращается в подвижную оокинету. Оокинета проникает в стенку кишечника комара и превращается в ооцисту. Ооциста растет, и содержимое ее делится, в результате чего образуется много спорозоитов. Процесс образования спорозоитов называется спорогонией. После разрыва ооцисты спорозоиты попадают в полость тела комара, а оттуда — в его слюнные железы. Дальнейшее развитие паразита продолжается в организме человека, куда спорозоиты попадают при укусе комара. Длительность спорогонии зависит от температуры окружающей среды и вида плазмодия. Высокие температуры значительно ускоряют спорогонию и обусловливают образование большого количества спорозоитов, а также вызывают более частое нападение комаров на человека. Диагностика. При лабораторной диагностике малярии достоверный диагноз можно поставить лишь при нахождении паразита методом микроскопического исследования крови больного. Для этого готовят мазок или толстую каплю крови, окрашивая их по Романовскому—Гимзе. Цитоплазма окрашивается в голубой цвет, ядро — в красный. Возможность обнаружения паразитов после окончания приступа уменьшается. Ретроспективная диагностика в настоящее время осуществляется путем применения серологических методов. Для определения видовой специфичности плазмодия применяют метод ПЦР. Профилактические мероприятия. Борьба с малярией состоит в выявлении и лечении больных, которые служат источником заражения комаров, а также в уничтожении комаров на всех этапах их биологического цикла развития. Для этого применяют инсектициды и биологические методы борьбы с комарами, а также проводят работы по осушению местности. Личная профилактика включает защиту от укусов комаров (использование репеллентов, москитных сеток). Проводят санитарно-просветительскую работу среди населения.
Токсоплазма (Toxoplasma gondii) — возбудитель токсоплазмоза, антропозооноза, природно-очаговой болезни. Заболевание распространено повсеместно. Toxoplasma gondii принадлежит к типу Apicomplexaи является единственным описанным видом рода Toxoplasma. Была открыта в 1908 г. французскими исследователями Ш. Николаем и Л. Мансе. Основные хозяева токсоплазмы — представители семейства кошачьих. В качестве промежуточных хозяев выступают различные виды теплокровных животных, в том числе и человек. Токсоплазмоз обычно протекает у человека легко. Однако для плода, в случае если мать заразилась токсоплазмозом во время беременности, а также для человека с пониженным иммунитетом эта болезнь может иметь серьезные последствия, вплоть до летального исхода. Жизненный цикл (Toxoplasma gondii) состоит из двух фаз. Половая часть жизненного цикла проходит только в особях некоторых видов семейства кошачьих (дикие и домашние кошки), которые становятся основным хозяином паразитов. Бесполая часть жизненного цикла может проходить в любом теплокровном животном, например в млекопитающих и птицах. В теле промежуточных хозяев паразит проникает в клетки, формируя так называемые межклеточные паразитофорные вакуоли, содержащие брадизоиты (медленно размножающиеся формы паразита). Внутри этих вакуолей T. gondii последовательно размножается делением на две части, до тех пор пока инфицированная клетка не разрушается и тахизоиты (активно размножающиеся формы паразита) выходят наружу. Тахизоиты подвижны и активно размножаются бесполым способом. В отличие от брадизоитов, свободные тахизоиты легко устраняются иммунной системой хозяина, но они могут проникнуть в клетки и сформировать брадизоиты, тем самым поддерживая инфекцию. При заражении токсоплазмозом клетки хозяина теряют способность образовывать фагосому, т. к. лизосомы не могут сливаться с вакуолью, где находится паразит. Вакуоли формируют тканевые цисты, в основном в мышцах и головном мозге. Поскольку паразит находится внутри клеток, то иммунная система хозяина не может обнаружить тканевые цисты. Тканевые цисты проглатываются кошкой (например, когда она съедает зараженную мышь). Цисты выживают в желудке кошки, и паразиты заражают эпителиальные клетки кишечника, где они размножаются половым способом и формируют ооцисты, которые выходят наружу с фекалиями. Животные (а также люди) проглатывают ооцисты (например, поедая немытые овощи и фрукты) или тканевые цисты (в плохо приготовленном мясе, сыром фарше) и заражаются. Паразиты внедряются в макрофаги в кишечном тракте и через кровь распространяются по организму хозяина.
Пути заражения человека. Для человека возможны три пути заражения токсоплазмозом: ¨ при употреблении недостаточно термически обработанного мяса, содержащего цисты (баранина, свинина); при контакте с загрязненными кошачьими испражнениями землей или песком; ¨ трансплацентарно — заражение плода от инфицированной матери во время беременности (врожденный токсоплазмоз); ¨ от инфицированных доноров при переливании крови лицам с ослабленным иммунитетом, а также при пересадке органов. Локализация. Токсоплазмы фиксируются в различных органах и тканях (печень, селезенка, нервная система, глаза, миокард сердца, легочный эпителий, скелетные мышцы). В этих органах образуются скопления паразитов в виде тканевых цист, которые могут сохраняться в организме десятки лет и даже пожизненно. Действие на организм человека. Заражение токсоплазмой в острой стадии может быть бессимптомным, но часто вызывает симптомы гриппа на ранних стадиях, как и грипп, может в редких случаях привести к смерти. Острая стадия спадает за период от нескольких дней до месяцев, переходя в хроническую стадию. Хроническая инфекция обычно бессимптомна, но в случае иммуноослабленных пациентов токсоплазмоз может развиваться в тяжелые формы. Наиболее частое проявление токсоплазмоза у иммуноослабленных пациентов — токсоплазмозный энцефалит, который может привести к смерти. Если заражение токсоплазмозом возникает во время беременности, то паразит может проникнуть через плаценту и заразить плод, что может привести к гидроцефалии, хориоретиниту (внутричерепному обызвествлению), а также к самопроизвольному аборту или внутриутробной смерти плода. Заражение токсоплазмозом во время беременности может привести к смерти новорожденного или тяжелым поражениям различных органов: нервной системы, глаз, конечностей.
Диагностика. Токсоплазмоз диагностируют с помощью серологических реакций (реакция связывания комплемента с токсоплазменным антигеном, метод флюоресцирующих антител, модификации ELISA, реакции с красителем, иммуноферментный анализ) или внутрикожной пробы с токсоплазмином. Профилактические мероприятия. Ветеринарный контроль домашних животных, ограничение контакта с кошками (особенно для беременных женщин), уничтожение грызунов, соблюдение правил личной гигиены, термическая обработка мяса, молока, яиц. Проведение санитарно-просветительской работы среди населения.
ТИП INFUSORIA (CILIOPHORA) Для инфузорий характерны постоянная форма тела и наличие пелликулы. Органеллами передвижения являются многочисленные реснички, которые покрывают всю клетку. Клетка инфузорий содержит два ядра: крупное — макронуклеус, регулирующее обмен веществ, и малое — микронуклеус, которое служит для обмена наследственной информацией при конъюгации. Инфузории имеют сложно организованный аппарат пищеварения: имеется цитостом — клеточный рот и цитофаринкс — клеточная глотка. Пищеварительные вакуоли перемещаются по эндоплазме, при этом пищеварительные ферменты выделяются поэтапно. Это обеспечивает полноценное переваривание пищи. Непереваренные остатки пищи выбрасываются через специальное образование — порошицу. У человека паразитирует единственная инфузория — балантидий, который обитает в толстом кишечнике. Балантидий(Balantidium coli) — возбудитель балантидиаза, антропозооноза. Паразитирует в организме человека и свиней. Балантидий впервые был обнаружен у свиней немецкими протозоологами Р. Лейкартом и Ф. Штейном в 1862 г. Паразит распространен повсеместно. Поскольку резервуаром для балантидия служат свиньи, балантидиаз чаще встречается у сельских жителей, которые занимаются свиноводством. Морфологические особенности. Балантидий существует в двух формах: трофозоита (вегетативная стадия) и цисты. Несимметричное овальное тело балантидия покрыто короткими ресничками, которые расположены продольными рядами. На переднем конце брюшной поверхности располагается перистом, который открывается наружу широким отверстием и заканчивается в клетке глоткой. Ротовое отверстие окружено длинными ресничками, которые продолжаются в глубину глотки. На заднем конце тела помещается перфорированное анальное отверстие. В цитоплазме находятся две сократительные вакуоли. Имеет два ядра: макронуклеус и микронуклеус. Размножается балантидий поперечным делением. Описан также половой процесс — конъюгация.
Цисты (Balantidium coli) диаметром около 50–60 мкм имеют округлую форму и окружены двойной оболочкой. В цитоплазме цисты сохраняется макронуклеус и сократительные вакуоли. Жизненный цикл. Балантидии в кишечнике свиней образуют цисты, которые выходят наружу с фекалиями. Заражение человека происходит перорально при проглатывании цист с загрязненными овощами, водой, с немытых рук (при забое свиней, использовании свиного навоза в качестве удобрения и при загрязнении им источников воды). Возможна передача инфекции от человека к человеку. Цисты могут распространяться мухами. Из проглоченных цист выходят трофозоиты, которые живут и размножаются в просвете толстого кишечника. Действие на организм человека. Во многих случаях заболевание протекает бессимптомно и развивается цистоносительство. У больных с клиническими проявлениями в стенке толстого кишечника находят такие же изменения, как при амебиазе, — поражение слизистой кишечника, язвы на стенках кишечника, развивается диарея. В отличие от амебиаза, при балантидиазе паразиты не распространяются в организме гематогенно. Диагностика. Обнаружение трофозоитов в фекалиях или биоптате толстого кишечника. Профилактические мероприятия. Выявление и лечение больных людей и цистоносителей. Личная гигиена: пить только кипяченую воду, соблюдать чистоту рук (особенно перед едой). Проводить ветеринарный контроль свиней на фермах, уничтожать мух. Санитарно-просветительская работа среди населения. |
















 Ядро округлое, крупное, при окраске по Романовскому—Гимзе цитоплазма голубовато-сиреневая, ядро и кинетопласт имеют красно-фиолетовую окраску. Размножаются простым делением.
Ядро округлое, крупное, при окраске по Романовскому—Гимзе цитоплазма голубовато-сиреневая, ядро и кинетопласт имеют красно-фиолетовую окраску. Размножаются простым делением. Обобщённая схема жизненного цикла лейшманий и эпидемиологических циклов лейшманиозов
Обобщённая схема жизненного цикла лейшманий и эпидемиологических циклов лейшманиозов