 ПОЗНАВАТЕЛЬНОЕ Сила воли ведет к действию, а позитивные действия формируют позитивное отношение Как определить диапазон голоса - ваш вокал Игровые автоматы с быстрым выводом Как самому избавиться от обидчивости Противоречивые взгляды на качества, присущие мужчинам Вкуснейший "Салат из свеклы с чесноком" Натюрморт и его изобразительные возможности Применение, как принимать мумие? Мумие для волос, лица, при переломах, при кровотечении и т.д. Как научиться брать на себя ответственность Зачем нужны границы в отношениях с детьми? Световозвращающие элементы на детской одежде Как победить свой возраст? Восемь уникальных способов, которые помогут достичь долголетия Классификация ожирения по ИМТ (ВОЗ) Глава 3. Завет мужчины с женщиной Оси и плоскости тела человека - Тело человека состоит из определенных топографических частей и участков, в которых расположены органы, мышцы, сосуды, нервы и т.д.
| Технология окислительной конверсии сероводорода в элементарную серу.
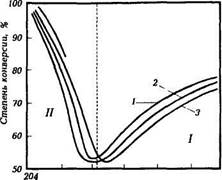
Технологический процесс предназначен для производства элементарной серы из кислого газа, полученного в процессе сероочистки природного газа. Процесс состоит из двух стадий: • производство серы в отделении Клаус; • производство серы в отделении Сульфрин. Исходное сырье — кислый газ с установок очистки газа; продукция — техническая газовая сера (ГОСТ 127-76). В кислых газах сера находится в связанном состоянии в виде сероводорода. Химизм процесса. Технологический процесс конверсии сероводорода в серу основан на зависимости Клауса и описывается реакцией: 2H2S + S02 3/п S + 2Н20 + Q, где п — количество атомов серы в молекуле, зависящее от температуры проведения реакции (и = 2 — 8). Эту стадию осуществляют в два этапа. На первом (термическом) этапе проводят сжигание сероводорода в воздухе. Поток кислого газа подается в печь, где смешивается с воздухом в соотношении 2: 1, и сжигается. Окисление происходит при температуре 900-1 350 «С. В реакцию вступает примерно 1/з H2S, содержащегося в газе. Продуктом окисления является диоксид серы S02: H2S + 3/п 02 — Н20+ S02 + Q По реакции 1 расходуется до 70 % масс, сероводорода и при этом выделяется значительное количество тепла, которое перед каталитической стадией должно быть утилизировано. Тепло, выделяющее Рис. 9.4. Зависимость степени конверсии H2S в серу от температуры при различном давлении паров в системе : 1-0,05 МПа; 2-0,1 МПа; 3-0,2 МПа; 4-0,1 МПа (из газа удалена вся сера); I - зона свободнопламен-ного горения; II - зона реакции на катализаторе Процесс термического окисления H2S осуществляют в основной топке, смонтированной в одном агрегате с котлом-утилизатором. Объем воздуха, поступающего в зону горения, должен быть строго дозирован, чтобы обеспечить для второй стадии требуемое соотношение SO2 и H2S (по стехиометрии реакции 2 оно должно быть 1:2). Температура продуктов сгорания при этом достигает 1100-1300 °С в зависимости от концентрации H2S и углеводородов в газе. Вывод серы из реакционной системы, образовавшейся при реакции 2, благоприятствует увеличению степени конверсии H2S до 95%. Поэтому стадию каталитической конверсии принято проводить в две ступени с выводом серы на каждой ступени. Зависимость степени конверсии H2S в серу от температуры и давления на обеих стадиях представлена на рис. 9.4. На графике показаны две зоны, разделенные пунктиром: высокотемпературная термического окисления (870-426 °С) и низкотемпературная каталитическая (426-204 °С). Элементная сера существует в различных модификациях - S2, S6 и S8: при высоких температурах газообразная сера в основном состоит из S2, а при снижении температуры она переходит в S6, затем в S8. Жидкая сера представлена преимущественно модификацией S8. В высокотемпературной зоне с повышением давления степень превращения H2S в серу снижается. В каталитической зоне повышение давления, наоборот, ведет к увеличению степени конверсии, так как давление способствует конденсации элементной серы и более полному выводу из зоны реакции. На практике увеличение степени конверсии H2S достигается применением двух или более реакторов-конверторов с удалением серы конденсацией и последующим подогревом газа между ступенями. При переходе от одного реактора к другому по потоку газа температуру процесса снижают. Традиционным катализатором в процессах Клауса вначале являлся боксит. На современных установках преимущественно применяют более активные и термостабильные катализаторы на основе из оксида алюминия. В печи наряду с основной реакцией протекают побочные реакции: С02 + H2S — COS + Н20 CH4 + 2S2 — 2H2S + CS2 Степень конверсии сероводорода на первой стадии достигает 55 %. Очищенные от серы газы поступают на вторую (каталитическую) стадию процесса. На этой стадии на катализаторе проходит окисление сероводорода диоксидом серы. На втором этапе газ проходит последовательно два каталитических конвертора, где % неокисленного H2S реагируют с S02 который образовался на первой стадии: 2H2S + S02 — 2Н20 + 3/п S + Q Полученные на первой стадии процесса сероорганические соединения подвергаются на катализаторе реакциям гидролиза с образованием сероводорода и диоксида углерода: CS2 + 2Н20 - 2H2S + С02 C0S + H20 -i - H2S + C02 В качестве катализатора используют оксид титана (ТO2) и окисноалюминиевый катализатор АД-К-1. Соотношение воздух : кислый газ выдерживается как 4:1. Суммарная степень очистки газа от сероводорода после прохождения термической и каталитической стадий достигает 95 %.
|



 ся по реакции 2 (1/5 от всего тепла), позволяет вести каталитический процесс при достаточно низких температурах и большой объемной скорости без системы съема тепла.
ся по реакции 2 (1/5 от всего тепла), позволяет вести каталитический процесс при достаточно низких температурах и большой объемной скорости без системы съема тепла.