ПОЗНАВАТЕЛЬНОЕ
| Окремі представники амінів 12
Метиламін СН3NH2 –газ із запахом аміаку, який розчиняється у воді та органічних розчинниках. Метиламін – продукт гниття білків. Використовують для синтезу деяких реактивів, фунгіцидів, інсектицидів, прискорювачів вулканізації каучуків, ПАР, лікарських препаратів. Диметиламін (СН3)2 NH – газ, який розчиняється у воді та органічних розчинниках. Утворюється при гнитті білків, особливо багато аміну є в складі оселедцевого розсолу. Триметиламін (СН3)3 N – газі з неприємним запахом, розчинний у воді й багатьох органічних розчинниках, утворюється при гнитті білків. Використовують при синтезі четвертинних сполук (бактерицидів), кормових домішок. Найбільше значення має хлорид триметилдодециламонію, який використовується як детергент, що має бактерицидні властивості, сировина для органічного синтезу. Кадаверин NH2 – (СН2)2 ‑ NH2 – безбарвна рідина, легко розчиняється у воді та етанолі. Відноситься до трупних отрут. Міститься в продуктах гниття білків, у мухоморах, ріжках. Утворюється при ферментативному декарбокислюванні амінокислоти лізину. Путресцин NH2 – (СН2)4‑ NH2 – кристалічна речовина, легко розчиняється у воді, етанолі, важче – в діетиловому етері. Відноситься до отрупних отрут. Утворюється при декарбокислюванні амінокислоти орнітину.. Використовують у синтезі деяких видів СВ. Гексаметилендіамін NH2 – (СН2)6 ‑ NH2 – безбарвна кристалічна речовина, гігроскопічна, добре розчинна у воді та етанолі. Застосовують для синтезу СВ найлону. Найлон – роговидний кристалічний полімер білого кольору, молекулярна маса – 15000 – 25000, плавиться при 2640С. Має високу міцність, волокно випускається вигляді безперервної нитки і штапелю. Використовують в текстильній промисловості для виготовлення різноманітних виробів. Анілін С6Н5 – NH2 – в’язка безбарвна рідина, темніє на повітрі і на світлі, слабко розчиняється у воді, краще – в етанолі та інших органічних розчинниках. Застосовують у синтезі барвників, медикаментів. Бензидин (4,4′-діамінодифеніл) NH2 – С6Н4 ‑ С6Н4 ‑ NH2 – біла кристалічна речовина, погано розчиняється у воді, краще в етанолі та діетиловому етері, швидко темніє на повітрі. Застосовують у біохімічному аналізу як реактив для виявлення крові в біологічних рідинах (сеча, травні соки), зм’якшувач гумової суміші, як реагент для визначення сульфатів, вольфраматів, у виробництві азобарвників, в колориметричному аналізу для визначення Сr, Cu, Fe, Pb, Hg. Бензидин ‑ канцерогенна речовина. * Ароматичні діазо- і азосполуки Діазосполуки – органічні речовини, в молекулах яких є азогрупа, що безпосередньо зв’язана з ароматичним радикалом:
Для азосполук характерна реакція азосполучення, яка дає можливість синтезувати багато органічних барвників. Азосполучення відноситься до реакцій електрофільного заміщення. Солі діазонію легко взаємодіють у слабколужному середовищі з фенолами, а у слабко кислому – з ароматичними амінами:
п-аміноазобензен (аніліновий жовтий) Азосполуки – органічні речовини в молекулі яких міститься азогрупа – N = N ‑, що зв’язана з двома ароматичними радикалами Аr. С6Н5 ‑ N = N – C6H5 ‑азобензен
Зміна кольору пов’язана зі зміною розподілу електронної густини в молекулі барвника. Так, при переході від лужного до кислого середовища відбувається протонування одного з атомів Нітрогену азогрупи барвника. При цьому із азогрупи – N = N –утворюється нова група – NН ‑ N= і змінюється будова ядра азоскладаючого фрагменту азобарвника – воно стає хіноїдним:
метиловий оранжевий в кислому середовищі (рожево-червоне забарвлення) Отже, забарвлення азобарвника залежить від наявності певних угруповань, при зміні реакції середовища змінюється структура молекул барвників та їх забарвлення.
Амінокислоти
Класифікація амінокислот
Номенклатура амінокислот Ä Тривіальна номенклатура (історичні назви): аргінін, лізин, гліцин. Ä Раціональна номенклатура. Вказують місце розміщення аміногрупи у вуглеводневому радикалі літерами грецького алфавіту (α, β, λ) + назва карбонової кислоти. Ä Номенклатура ІЮПАК. Цифрами вказують місце розміщення аміногрупи і радикала + назва кислоти (за вуглеводнем):
Ізомерія амінокислот ü ізомерія карбонового радикала:
2-амінобутанова кислота 2-аміно-2-метилпропанова кислота ü ізомерія по місцеположенню в радикалі аміногрупи:
2-амінобутанова кислота 3-амінобутанова кислота ü оптична ізомерія (крім гліцину):
оптичні ізомери аланіну Фізичні властивості Амінокислоти – безбарвні кристалічні речовини, добре розчинні у воді, мають високі температури плавлення, можуть розкладатися. Кристалізуються з розчинів у вигляді біполярних іонів. Більшість D-амінокислот солодкі, L-амінокислоти гіркі або без смаку. Хімічні властивості Амінокислоти – амфотерні сполуки (взаємодія з мінеральними кислотами і лугами з утворенням солей):
B aмінoкиcлотax містяться дві іоногенні групи тому їх сyмapний зapяд залежить від значення pH середовища.
NH2 – CH2 – COOH ↔ +NH3 – CH2 – COO- гліцин внутрішня сіль гліцину(цвіттер-іон) *В молекулі гістидину поряд з карбоксильною та аміногрупою наявний імідазольний залишок. Тому при підвищенні рН середовища заряд гістидину змінюється від +2 до -1. При рН = 7,6 сумарний заряд дорівнює нулю, незважаючи на наявність двох повністю іонізованих груп в молекулі гістидину. Величина рН, при якій сумарний заряд дорівнює нулю, називається ізоелектричною точкою. В ізоелектричній точці гістидин є цвіттер-іоном, тобто молекула виявляє властивості як аніона так і катіона. B нейтральній області рН більшість амінокислот також є цвіттер-іонами.
Завдання. Визначити реакцію середовища в розчині амінокислоти:
1. Амфотерні властивості (взаємодія з мінеральними кислотами та основами з утворенням солей). Ä Утворення солей з кислотами NH2 – CH2 – COOH + НСІ → [+NH3 – CH2 – COOH] CI-(хлорид гліцину) Ä Утворення солей з основами:звичайних солей з лугами та внутрішньо комплексних солей з купрумом (ІІ) інтенсивно-синього кольору:
внутрішньокомплексна сіль амінокислоти 2. Утворення естерів (взаємодія зі спиртами):
Реакцію використовують для розділення і виділення амінокислот із білкових гідролізатів. 3. Утворення хлорангідридів відбувається при взаємодії амінокислот з пентахлоридом фосфору РСІ5, утворюються хлорангідриди амінокислот. Вони нестійкі і існують тільки у вигляді солей:
Реакція декарбоксилювання
аланін етиламін Ферментативна реакція, що відбувається в клітинах живих організмів під впливом ферментів декарбоксилаз. 5. Дезамінування амінокислот відбувається під впливом нітритноїкислоти або ферментів дезамінази:
гліцин нітритна кислота гліколева кислота
аланін лактатна (молочна) кислота Окислювальне дезамінування відбувається під впливом окислювачів (гіпохлорити, хлорамін Т, персульфати), утворюються кетокислоти:
Реакція окислювального дезамінування відбувається в організмах людини і тварин під впливом специфічних ферментів. *Для якісного і кількісного визначення амінокислот використовується нінгідрин. При нагріванні з амінокислотою відбувається відновлення нінгідрину до дикетооксигідриндену, а амінокислота розщеплюється на альдегід, вуглекислий газ і аміак:
Внаслідок конденсації аміаку з молекулами нінгідрону та дикетооксигідриндену відбувається утворення амонійної солі, що забарвлена в синьо-фіолетовий колір:
Ацилювання амінокислот Амінокислоти реагують з хлорангідридами та ангідридами кислот з утворенням N-ацильованих похідних. Реакція відбувається до кінця тільки у водно-лужних або неводних середовищах так як у взаємодію вступає амінна група:
ацетилхлорид гліцин N-ацетилгліцин N-Ацильовані похідні амінокислот використовуються при синтезі пептидів. Окремі ацильовані амінокислоти здатні знешкоджувати отруйні речовини, які всмоктуються у кров з кишківника. Так, наприклад, отруйна бензойна кислота зв’язується з гліцином та видаляється з організму з сечею в формі гіпурової кислоти:
бензойна кислота гліцин гіпюрова кислота 12 |




 діазобензен хлорид
діазобензен хлорид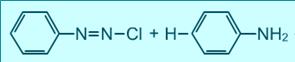








 HOSO3 ‑ ─ NH ─ N ═ ═ N+ CI-
HOSO3 ‑ ─ NH ─ N ═ ═ N+ CI- СН3
СН3















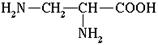




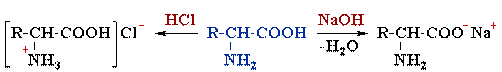



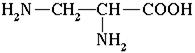



 натрієва сіль амінокислоти
натрієва сіль амінокислоти

 амінооцтова кислота етанол етилгліциноат (етиловий естер гліцину)
амінооцтова кислота етанол етилгліциноат (етиловий естер гліцину)


 СН3 – СНNH2 – COOH + H2O CH3 – CHOH – COOH + NH3
СН3 – СНNH2 – COOH + H2O CH3 – CHOH – COOH + NH3